题目内容
【题目】某研究性学习小组为确定某蜡状有机物A的结构和性质,他们拟用传统实验的手段与现代技术相结合的方法进行探究。请你参与探究过程:
Ⅰ.实验式的确定
(1)取样品A进行燃烧法测定。发现燃烧后只生成CO2和H2O,某次燃烧后,经换算得到了0.125 mol CO2和2.7g H2O。据此得出的结论是_______;
(2)另一实验中,取3.4 g蜡状A在3.36 L(标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成2.8 L CO2和液态水。通过计算确定A的实验式;__________
Ⅱ.结构式确定(经测定A的相对分子质量不超过140)
(3)取少量样品熔化,加入钠有氢气放出,说明A分子中含有_______基;
(4)进行核磁共振,发现只有两个特征峰,且面积比为8:4,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收。图谱如下:
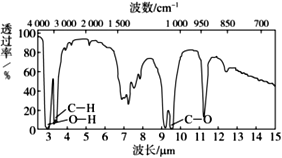
则A的结构简式为_______;
Ⅲ.性质探究
(5)A与浓氢溴酸混合加热发生反应的化学方程式为_______________。
【答案】n(H2O)=2.7g/18g·mol-1 = 0.15mol,N(C): N(H)= n(CO2): n(H2O)×2=0.125 mol: 0.15 mol×2=5:12,A中可能含有O,分子中n(C)∶n(H)=5∶12,实验式为C5H12Oz(z=0,1,2,…) n(CO2)=2.8L/22.4L·mol-1=0.125 mol,与(1)中产生的CO2等量,则产生的水n(H2O)=0.15 mol,(依据质量守恒定律求算也可) n(O)=![]() 0.1mol,N(C): N(H): N(O)= 0.125 mol: 0.15 mol×2: 0.1 mol=5:12:4,则A的实验式:C5H12O4 羟 C(CH2OH)4 C(CH2OH)4+4HBr
0.1mol,N(C): N(H): N(O)= 0.125 mol: 0.15 mol×2: 0.1 mol=5:12:4,则A的实验式:C5H12O4 羟 C(CH2OH)4 C(CH2OH)4+4HBr ![]() C(CH2Br)4+4H2O
C(CH2Br)4+4H2O
【解析】
燃烧产物只有CO2和H2O,则样品中一定有C、H元素,可能有O元素。据样品、CO2和H2O的质量,可计算确定有无氧元素、求得实验式。再由实验式、相对分子质量求出有机物的分子式。最后,根据有机物的化学特性、波谱特征,推断有机物的结构。
(1)燃烧产物只有CO2和H2O,则样品中一定有C、H元素,可能有O元素。n(C)=n(CO2)=0.125 mol,n(H)=n(H2O)×2=(2.7g/18g·mol-1)×2 = 0.3mol,则N(C): N(H)= n(CO2): n(H)=0.125 mol: 0.3 mol=5:12,A实验式为C5H12Oz(z=0,1,2,…)。
(2)n(CO2)=2.8L/22.4L·mol-1=0.125 mol,与(1)中CO2等量,则n(H2O)=2.7g/18g·mol-1=0.15 mol,n(O)= ![]() 0.1mol,N(C): N(H): N(O)= 0.125 mol: 0.15 mol×2: 0.1 mol=5:12:4,则A的实验式C5H12O4;
0.1mol,N(C): N(H): N(O)= 0.125 mol: 0.15 mol×2: 0.1 mol=5:12:4,则A的实验式C5H12O4;
(3)设A分子式(C5H12O4)n,则Mr=136n<140,仅n=1合理,即A分子式为C5H12O4。A与钠反应放出氢气,说明A分子中含有羟基(A分子中氢原子数已饱和,不可能有羧基);A核磁共振只有两个吸收峰、且面积比为8:4,即A分子中有两种氢原子且数目之比为8:4;红外光谱图说明A分子中有C-H、O-H、C-O键,故A结构简式为C(CH2OH)4。
(5)A与浓氢溴酸加热时,羟基被溴原子取代,反应的化学方程式C(CH2OH)4+4HBr ![]() C(CH2Br)4+4H2O。
C(CH2Br)4+4H2O。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案