题目内容
11.下列说法中,错误的是( )| A. | 乙烯是重要的工业燃料和民用燃料 | |
| B. | 乙烯可以催熟果实 | |
| C. | 乙烯分子里双键中的一个键容易被氧化而断裂 | |
| D. | 乙烯聚合成聚乙烯,聚乙烯也能发生加成反应 |
分析 A.乙烯是重要的化工原料;
B.乙烯对植物生长具有调节作用;
C.乙烯碳碳双键中的一个键键能较小,容易断裂;
D.聚乙烯不含不饱和键.
解答 解:A.乙烯是重要的工业燃料和民用燃料,不用作燃料,故A错误;
B.乙烯对植物生长具有调节作用,能够促进果实成熟,故B正确;
C.乙烯碳碳双键中的一个键键能较小,容易断裂,容易发生加成和氧化反应,故C正确;
D.聚乙烯不含不饱和键,不能发生加成反应,故D错误;
故选:AD.
点评 本题考查了乙烯的性质与用途,熟悉乙烯的结构及化学性质是解题关键,题目难度不大.

练习册系列答案
相关题目
1.下列装置能构成原电池的是 ( )
| A. | 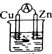 乙醇 | B. |  稀H2SO4 | C. | 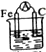 稀HCl | D. | 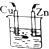 稀H2SO4 |
2.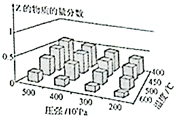 为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验的到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验的到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
 为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验的到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验的到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )| A. | 在恒温恒容条件下,向已达到平衡的体系中加入少量Z,平衡正向移动,Z的含量增大 | |
| B. | 升高温度,正、逆反应速率都增大,平衡常数增大 | |
| C. | △H<0 m+n>c | |
| D. | △H>0 m+n<c |
19.W、X、Y、Z为四种短周期元素,X、Z同主族,已知X的原子半径大于Z的原子半径,W的最高正价氧化物对应水化物比Y的最高价氧化物对应水化物的碱性强,Y的阳离子、W的阳离子、Z的阴离子具有相同的电子层结构,下列叙述正确的是( )
| A. | 原子半径:W>X>Y>Z | |
| B. | 单质与盐酸反应速率:Y>W | |
| C. | X最低价氢化物的稳定性强于Z最低价氢化物 | |
| D. | 原子序数:X>W>Y>Z |
6.在能使酚酞变红的无色溶液中,可大量共存的离子组是( )
| A. | Na+、Cu2+、Br-、Cl- | B. | K+、NH4+、Cl-、Na+ | ||
| C. | K+、Na+、NO3-、H+ | D. | K+、S2-、SO42-、OH- |
16.某气态烷烃和一气态单烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48L,通入足量的溴水,溴水的质量增加2.8g,此2种烃是( )
| A. | 甲烷和丙烯 | B. | 甲烷和2-丁烯 | ||
| C. | 甲烷和2-甲基丙烯 | D. | 乙烯和1-丁烯 |
3.下列描述对象所含分子数由多到少的排列顺序是( )
①3g H2
②所含电子的物质的量为4mol的H2
③45g H2O
④常温下,16g O2与14g N2的混合气体
⑤含原子总数约为1.204×1024的NH3.
①3g H2
②所含电子的物质的量为4mol的H2
③45g H2O
④常温下,16g O2与14g N2的混合气体
⑤含原子总数约为1.204×1024的NH3.
| A. | ①②③④⑤ | B. | ③②①④⑤ | C. | ③②⑤①④ | D. | ②③①④⑤ |
10.当光束通过下列分散系时,能产生丁达尔效应的是( )
| A. | CuSO4溶液 | B. | NaOH溶液 | C. | Fe(OH)3胶体 | D. | HCl溶液 |