题目内容
2.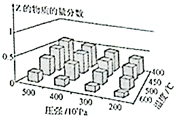 为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验的到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验的到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )| A. | 在恒温恒容条件下,向已达到平衡的体系中加入少量Z,平衡正向移动,Z的含量增大 | |
| B. | 升高温度,正、逆反应速率都增大,平衡常数增大 | |
| C. | △H<0 m+n>c | |
| D. | △H>0 m+n<c |
分析 由图象可知,降低温度,Z的物质的量分数增大,说明降低温度平衡向正反应方向移动,所以正反应是放热的,则△H<0,
降低压强,Z的物质的量分数减小,说明压强减小,平衡向着逆反应方向移动,减小压强,化学平衡是向着气体系数和增加的方向进行的,所以有m+n>c,由此分析解答.
解答 解:由图象可知,降低温度,Z的物质的量分数增大,说明降低温度平衡向正反应方向移动,所以正反应是放热的,则△H<0,
降低压强,Z的物质的量分数减小,说明压强减小,平衡向着逆反应方向移动,减小压强,化学平衡是向着气体系数和增加的方向进行的,所以有m+n>c,
A、在恒温恒容条件下,向已达到平衡的体系中加入少量Z,相当于增大压强,平衡逆向移动,但Z的含量增大,故A错误;
B、升高温度正逆反应速率都加快,但因正反应是放热反应,所以平衡常数减小,故B错误;
C、正反应是放热的,则△H<0,减小压强,化学平衡是向着气体系数和增加的方向进行的,所以有m+n>c,故C正确;
D、由C知,△H<0 m+n>c,故D错误;故选C.
点评 本题考查温度、压强等外界条件对平衡移动的影响,题目难度中等,解答本题的关键是能正确分析图象曲线的变化趋势.

练习册系列答案
相关题目
13.下列运用与碳酸钠或碳酸氢钠能发生水解的事实无关的是( )
| A. | 实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 | |
| B. | 泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将其混合就可产生大量二氧化碳的泡沫 | |
| C. | 将稀盐酸逐滴加入到Na2CO3溶液中,开始无二氧化碳放出 | |
| D. | 可用碳酸钠与醋酸制取少量二氧化碳 |
7. 已知元素X,Y,Z在周期表中的相对位置如图所示,Y元素基态原子的价电子排布为nsn-1npn+1,则下列说法错误的是( )
已知元素X,Y,Z在周期表中的相对位置如图所示,Y元素基态原子的价电子排布为nsn-1npn+1,则下列说法错误的是( )
 已知元素X,Y,Z在周期表中的相对位置如图所示,Y元素基态原子的价电子排布为nsn-1npn+1,则下列说法错误的是( )
已知元素X,Y,Z在周期表中的相对位置如图所示,Y元素基态原子的价电子排布为nsn-1npn+1,则下列说法错误的是( )| A. | X元素所在周期中所含非金属元素最多 | |
| B. | Z元素基态原子的核外电子排布式为[Ar]3d104s24p3 | |
| C. | Y的氧化物空间构型可能为V型 | |
| D. | 三种元素的最高价氧化物对应水化物酸性最强的是X |
14.下列各组物质的晶体中,化学键类型、晶体类型都相同的是( )
| A. | CO2和SiO2 | B. | C60和晶体硅 | C. | KCl和HCl | D. | CO2和H2O |
11.下列说法中,错误的是( )
| A. | 乙烯是重要的工业燃料和民用燃料 | |
| B. | 乙烯可以催熟果实 | |
| C. | 乙烯分子里双键中的一个键容易被氧化而断裂 | |
| D. | 乙烯聚合成聚乙烯,聚乙烯也能发生加成反应 |

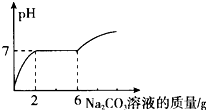 在烧杯中盛有10g HCl和BaCl2的混合溶液,向其中逐滴滴入溶质质量分数为13.25%的碳酸钠溶液.测得溶液pH与加入的碳酸钠溶液的质量关系如图所示.
在烧杯中盛有10g HCl和BaCl2的混合溶液,向其中逐滴滴入溶质质量分数为13.25%的碳酸钠溶液.测得溶液pH与加入的碳酸钠溶液的质量关系如图所示. 2,3-二甲基戊烷
2,3-二甲基戊烷 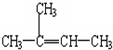 2-甲基-2-丁烯
2-甲基-2-丁烯