题目内容
1.下列装置能构成原电池的是 ( )| A. | 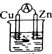 乙醇 | B. |  稀H2SO4 | C. | 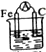 稀HCl | D. | 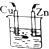 稀H2SO4 |
分析 根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
解答 解:A、乙醇不是电解质,锌和酒精不能自发的进行氧化还原反应,所以不能构成原电池,故A错误;
B、没有两个活泼性不同的电极,所以不能构成原电池,故B错误;
C、该装置符合原电池的构成条件,所以能形成原电池,故C正确;
D、该装置不能构成闭合回路,所以不能构成原电池,故D错误;
故选C.
点评 本题考查了原电池的构成条件,难度不大,注意这几个条件必须同时存在才能形成原电池,缺一不可.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
11.一定条件下,用如图所示装置可实现有机物的储氢,下列有关说法正确的是( )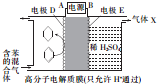

| A. | 电子流向:D→A,B→E | |
| B. | 气体X为O2 | |
| C. | 电极D为惰性电极,E为活泼电极 | |
| D. | 电极D的电极反应式为C6H6+6H++6e-═C6H12 |
16.下表是元素周期表的一部分,请针对表中的①~⑨号元素回答问题.
(1)写出⑦的原子结构示意图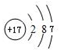 .
.
(2)最活泼的金属元素是K(填元素符号,下同);化学性质最稳定的元素是Ne.
(3)第三周期元素形成的气态氢化物中,最稳定的氢化物是HCl(填化学式).
(4)①的最高价氧化物中化学键的类型属于共价键.
(5)用电子式表示④与⑥组成的A2B型化合物的形成过程: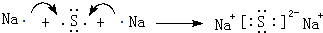 .
.
(6)⑤的最高价氧化物属于两性氧化物,它与氢氧化钠反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
(7)②的单质与H2反应的化学方程式为N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ⑧ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 4 | ⑨ |
 .
.(2)最活泼的金属元素是K(填元素符号,下同);化学性质最稳定的元素是Ne.
(3)第三周期元素形成的气态氢化物中,最稳定的氢化物是HCl(填化学式).
(4)①的最高价氧化物中化学键的类型属于共价键.
(5)用电子式表示④与⑥组成的A2B型化合物的形成过程:
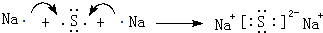 .
.(6)⑤的最高价氧化物属于两性氧化物,它与氢氧化钠反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
(7)②的单质与H2反应的化学方程式为N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
6.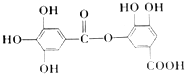 有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
 有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )| A. | 有弱酸性,1mol该有机物与溴水反应,最多能消耗4mol Br2 | |
| B. | 在一定条件下,1mol该物质最多能与6mol NaOH完全反应 | |
| C. | 在Ni催化下,1mol该物质可以和7mol H2发生加成反应 | |
| D. | 它能发生水解反应,水解后只能生成两种产物 |
13.下列运用与碳酸钠或碳酸氢钠能发生水解的事实无关的是( )
| A. | 实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 | |
| B. | 泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将其混合就可产生大量二氧化碳的泡沫 | |
| C. | 将稀盐酸逐滴加入到Na2CO3溶液中,开始无二氧化碳放出 | |
| D. | 可用碳酸钠与醋酸制取少量二氧化碳 |
11.下列说法中,错误的是( )
| A. | 乙烯是重要的工业燃料和民用燃料 | |
| B. | 乙烯可以催熟果实 | |
| C. | 乙烯分子里双键中的一个键容易被氧化而断裂 | |
| D. | 乙烯聚合成聚乙烯,聚乙烯也能发生加成反应 |
 .
.
