题目内容
15.检验未知溶液中是否含有SO${\;}_{4}^{2-}$,下列操作中最合理的是( )| A. | 加入硝酸酸化的硝酸钡溶液 | B. | 先加硝酸酸化,再加入硝酸钡溶液 | ||
| C. | 加盐酸酸化了的BaCl2溶液 | D. | 先加盐酸酸化,再加入BaCl2溶液 |
分析 SO42-的检验的方法为:先向溶液中加稀盐酸,然后再加氯化钡溶液,若生成白色沉淀,则溶液中有SO42-.在检验时要注意排除SO32-、CO32-等离子的影响.
解答 解:检验 SO42- 时要避免 SO32- 的影响,就不要加入稀硝酸,因为稀硝酸能把SO32- 氧化为SO42-,从而干扰SO42- 的检验,故AB错误;
若将盐酸和氯化钡一同加入,则生成的白色沉淀除了可能是BaSO4,还可能是AgCl,即加入盐酸酸化的氯化钡不能排除Ag+的干扰,故C错误;
故要先加入过量稀盐酸,以除去Ag+、SO32-、CO32- 等离子的影响,然后再价氯化钡,若有白色沉淀产生,则证明有SO42-.
故选D.
点评 本题考查了SO42-的检验,应注意何时加入盐酸能确保排除Ag+、SO32-、CO32- 等离子的影响,难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
10.蔗糖晶体中滴2~3滴水,再滴入适量的浓硫酸.发现加水处立即变黑,黑色区不断扩大,最后变成一块疏松的焦炭,并伴有刺激性气味气体产生,该实验中浓硫酸表现的性质有( )
①.溶于水放出大量热 ②高沸点难挥发 ③酸性 ④强氧化性 ⑤吸水性 ⑥脱水性.
①.溶于水放出大量热 ②高沸点难挥发 ③酸性 ④强氧化性 ⑤吸水性 ⑥脱水性.
| A. | ①②③④ | B. | ①②⑤⑥ | C. | ①④⑤⑥ | D. | ③④⑤⑥ |
20.下列反应中,反应物量的相对多少都会影响反应产物,下列离子方程式正确的是( )
| A. | 少量CO2通入过量氨水中:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 含等物质的量的NH4HSO3与NaOH溶液混合加热:HSO3-+OH-$\frac{\underline{\;△\;}}{\;}$SO32-+H2O | |
| C. | 溴化亚铁溶液中通入少量Cl2:Cl2+2Br-═2Cl-+Br2 | |
| D. | 含1molKOH的溶液与含2molBa(HCO3)2的溶液混合:Ba2++2HCO3-+2OH-═BaCO3↓+CO32-+2H2O |
7.下列实验操作中错误的是( )
| A. | 试用分液漏斗分液时,应将漏斗颈上的玻璃塞打开 | |
| B. | 蒸馏实验不一定使用温度计 | |
| C. | 用CCl4萃取碘水中的碘 | |
| D. |  过滤(如图)时,可将悬浊液从烧杯直接倒入漏斗中 过滤(如图)时,可将悬浊液从烧杯直接倒入漏斗中 |
15.工业接触法制硫酸没有涉及的设备是( )
| A. | 沸腾炉 | B. | 接触室 | C. | 高炉 | D. | 吸收塔 |
 反应类型:加聚反应
反应类型:加聚反应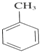 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$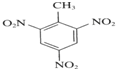 +3H2O.
+3H2O.