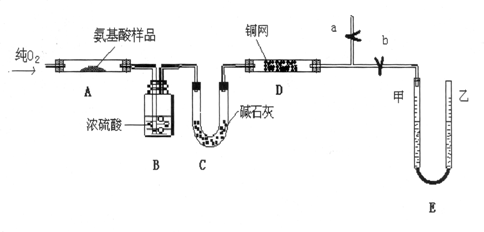
题目内容
10.用如图所示的装置进行电解,通电一段时间后,发现Pt电极上有气泡冒出.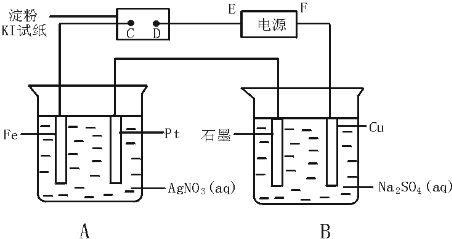
(1)E为电源的负极,通电时铜电极上发生的电极反应为Cu-2e-=Cu2+.
(2)A中发生反应的离子方程式为:4Ag++2H2O=4Ag+O2↑+4H+.
(3)室温下,若从电解开始到时间为t s,A、B装置共收集到气体0.0075mol,若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为100mL,则A溶液的pH为1.
分析 由pt电极上有气泡冒出可知Pt为阳极,生成氧气,则E为负极,F为正极,A中Fe为阴极,B中铜为阳极,A池的电极反应分别是:阴极电极反应(左边):Ag++e-→Ag;阳极电极反应(右边):4OH-→2H2O+O2↑+4e-,池的电极反应分别是:阴极电极反应(左边):2H++2e-=H2↑;阳极电极反应(右边):Cu-2e-=Cu2+,结合电极方程式解答该题.
解答 解:(1)由pt电极上有气泡冒出可推断E为电源的负极,B中铜为阳极,被氧化生成Cu2+,电极方程式为Cu-2e-=Cu2+,
故答案为:负;Cu-2e-=Cu2+;
(2)A池的电极反应分别是:阴极电极反应(左边):Ag++e-→Ag;阳极电极反应(右边):4OH-→2H2O+O2↑+4e-
总反应:4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3,离子方程式:4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4H+,
故答案为:4Ag++2H2O=4Ag+O2↑+4H+;
(3)A中发生4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4H+,B中发生Cu+2H2O$\frac{\underline{\;通电\;}}{\;}$Cu(OH)2↓+H2↑,
得到关系式:2H2~O2~3(总气体--氢气和氧气)~4H+
2x x 3x 4x
3x=0.0075mol,则4x=0.01mol,
c(H+)=$\frac{0.01mol}{0.1L}$=1mol/L,
pH=1,
故答案为:1.
点评 本题综合考查电解池知识,为高频考点,侧重于学生的分析、计算能力的考查,注意把握原电池、电解池的工作原理以及电极、电解方程式的书写,结合反应的方程式计算,难度不大.

| A. | 苯中的甲苯(溴水、分液) | B. | 溴乙烷中的乙醇(水、分液) | ||
| C. | 乙醇中的水(CaO、蒸馏) | D. | 溴苯中的溴(NaOH溶液、分液) |
| A. | K2SO4•2Cr2(SO4)3 | B. | 2K2SO4•Cr2(SO4)3 | C. | K2SO4•Cr2(SO4)3 | D. | K2SO4•$\frac{1}{2}$Cr2(SO4)3 |
| A. | 蛋白质 | B. | 油脂 | C. | 淀粉 | D. | 聚乙烯 |
| A. | HCl溶于水 | B. | 干冰升华 | ||
| C. | 固体NaCl熔融 | D. | 煤矿中瓦斯(主要成分CH4)遇火爆炸 |
| Ⅰ除杂实验 | Ⅱ试剂 | Ⅲ操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯酚) | A.饱和Na2CO3溶液 B.NaCl晶体 C.NaOH溶液 D.CaO | a.蒸馏 b.分液 c.盐析、过滤 d.萃取 | ① | ||
| ②乙醇(水) | ② | ||||
| ③肥皂(甘油、水) | ③ | ||||
| ④乙酸乙酯(乙酸) | ④ | ||||
b.向a中所得的银氨溶液中滴入少量葡萄糖溶液,混合均匀后,放在水浴中加热3min~5min,即可在试管内壁上形成银镜,则此反应的化学方程式为(葡萄糖的结构简式用G-CHO表示):③G-CHO+2Ag(NH3)2OH$\stackrel{△}{→}$G-COONH4+2Ag↓+3NH3+H2O.
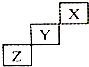
| A. | X是种活泼的非金属元素 | |
| B. | Z的最高价氧化物的水化物是一种弱酸 | |
| C. | Y的氢化物很稳定 | |
| D. | Y元素的最高化合物为+7价 |
| A. | 化学式为CF2Cl2的物质可以看作是甲烷的衍生物,它有两种分子结构 | |
| B. | 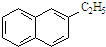 所有原子都处于同一平面 所有原子都处于同一平面 | |
| C. | C3H8O有2种同分异构体 | |
| D. | 甲苯的二氯代物共有10种 |