题目内容
1.实验室用燃料法测定某种氨基酸(CxHyOzNp)的分子式组成,取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.现用如图所示装置进行实验(铁架台、铁夹、酒精灯等未画出).请回答有关问题: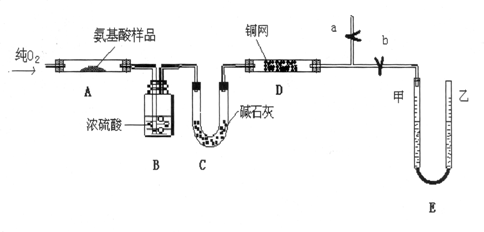
(1)实验开始前,按图装好装置,检验装置气密性,打开止水夹b,关闭止水夹a,向装置中通入一定量氧气,并封闭进气口,若观察到E装置管内液面甲低乙高,并维持不变.,则证明装置气密性良好.
(2)打开止水夹a后,再关闭止水夹b,通入一段时间的纯氧,通入氧气的目的是赶走装置内的空气(或氮气).,之后关闭止水夹a,打开止水夹b.
(3)加热A、D,缓缓通入纯氧,使氨基酸样品发生燃烧,装置D中的铜网的作用是除去氧气,实验前后需要通过称量获取相关数据的装置是BC.
(4)E装置的作用是测量氮气的体积,并由此确定待测氨基酸中含有的氮元素(或N)的质量,为了较准确地测量该气体的体积.在读反应前后甲管中液面的读数求其差值的过程中,应注意ac(填代号).
a.视线与粗细蓝线的交界点相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(5)氨基酸燃烧完全后,是否需要继续通入氧气是(填“是”或“否”),其理由是将滞留在装置中的CO2、H2O、N2赶入相应的检测装置,确保测量数据的准确..
分析 该实验原理为:Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2.通过测定CO2、H2O和N2的质量,确定分子中三种元素原子个数比,由此确定最简式.
(1)气密性的检查,要注意液面是否变化,根据气压原理来检验装置的气密性;
(2)该题利用氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2,测定某种氨基酸(CxHyOzNp)的分子式组成所以题目中注意除去N2;
(3)最后测定氮气体积时,还要除去过量的氧气,反之在元素的测定上造成干扰,在测量气体的体积时注意压强;
(4)氮气的含量可以根据排水法来确定,注意测定时保持压强与大气相同故选一段时间,保持甲、乙两管液面相平;
(5)为保证实验数据的准确性,氨基酸燃烧完全后,需要继续通入氧气,将滞留在装置中的CO2、H2O、N2赶入相应的检测装置.
解答 解:(1)打开止水夹b,关闭止水夹a,向装置中通入一定量氧气,并封闭进气口若漏气会使两面液体相平,
故答案为:E装置管内液面甲低乙高,并维持不变;
(2)该题利用氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2,测定某种氨基酸(CxHyOzNp)的分子式组成,通氧气为赶走影响测定的氮气,
故答案为:赶走装置内的空气(或氮气);
(3)装置D中的铜网的作用是除去氧气,防止测量的氮气体积不准,实验前后需要通过称量获取相关数据的装置是:B测得水的量、C测得二氧化碳的量,
故答案为:除去氧气,BC;
(4)保持压强与大气相同故选一段时间,并保持甲、乙两管液面相平.
故答案为:氮气,氮元素(或N),ac;
(5)氨基酸燃烧完全后,需要继续通入氧气,确保CO2、H2O、N2进入后面的装置.
故答案为:是,将滞留在装置中的CO2、H2O、N2赶入相应的检测装置,确保测量数据的准确.
点评 类似实验题注意气密性的检查、实验数据的准确性、还有实验时的细节、数据的测定方法处理等等.

| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| B. | 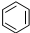 +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$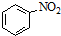 +H2O +H2O | |
| C. | CH3CH2OH+CH3COOH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| D. | CH2=CH2+HBr→CH3CH2Br |
| A. | 反应过程中I2置换出Cl2,由此可推断非金属性I>Cl | |
| B. | 反应中I2为氧化剂,Cl2为氧化产物 | |
| C. | 生成1 mol Cl2时转移2 mol电子 | |
| D. | 由方程式可知还原性I2>Cl2 |
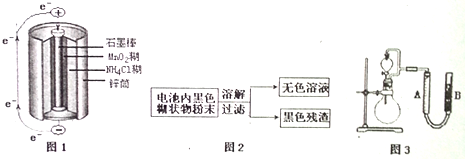
(1)图1是锌锰干电池基本构造图,该电池的负极材料是Zn;工作时NH4+离子在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是2NH4++2e-═2NH3↑+H2↑;当电路中每通过0.2mole-,负极质量减少6.5g;
(2)图2是利用废旧锌锰干电池内的黑色糊状物分离得到黑色残渣MnO2的流程图.该流程中溶解和过滤操作均要使用到的玻璃仪器有烧杯和玻璃棒;
(3)图3是探究MnO2在制O2过程中的作用的实验装置图,利用该装置完成下表中实验一和实验二,实验过程中有关实验现象和所得数据如下表(已知:两次实验气体的体积在相同条件下测定:H2O2由分液漏斗滴入到圆底烧瓶).
| 序号 | 烧瓶中的物质 | 实验记录 | 实验结论 |
| 实验一 | 足量MnO2 | a.充分反应后未见黑色固体物质减少 b.收集到112mL气体 | ①催化剂 |
| 实验二 | 足量MnO2和稀硫酸 | c.充分反应后黑色粉末部分溶解 d.收集到112mL气体 | ②氧化剂 |
④实验一、二中参加反应的H2O2的物质的量之比为2:1.
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
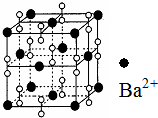 钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如图所示,有关说法正确的是( )
钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如图所示,有关说法正确的是( )| A. | 该晶体为分子晶体 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 该氧化物的电子式为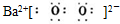 | |
| D. | 与每个Ba2+距离相等且最近的Ba2+共有6个 |
| A. | 电池的电解液为碱性溶液,负极为Fe | |
| B. | 电池放电过程中,正极附近溶液的pH增大 | |
| C. | 电池放电时,电解质溶液中OH-移向正极 | |
| D. | 电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| A. | 1H、2H、3H、H2都是氢元素的同位素 | |
| B. | 同种元素的原子,质量数一定相同 | |
| C. | 互为同位素的原子,质子数一定相同 | |
| D. | 由一种元素组成的物质,一定是纯净物 |