题目内容
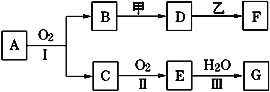
【题目】物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A是一种能使红色石蕊试液变蓝的气体,甲为淡黄色固体化合物,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化,用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成。请回答下列问题:
(1)写出甲的电子式是___________;
(2)写出反应Ⅰ的化学方程式__________;
(3)A溶于水得到溶液X,在25℃下,将a mol·L-1的X与b mol·L-1的G溶液等体积混合,溶液显中性,则所得溶液中离子浓度由大到小的顺序为______________;用含a和b的代数式表示出该混合溶液中X的电离平衡常数_______________________。
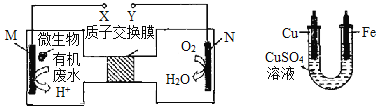
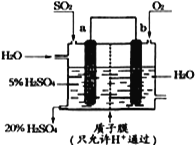
(4)工业上采用的一种污水处理方法是:保持污水的pH在5.0~6.0之间,通过如图装置处理污水。
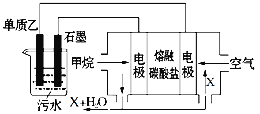
① 电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:Ⅰ.___; Ⅱ.______。
② 为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分X物质参加循环,X物质的化学式是_______________________。
【答案】![]() 4NH3+5O2
4NH3+5O2 ![]() 4NO+6H2O c(NO3—)=c(NH4+)>c(OH—)= c(H+)
4NO+6H2O c(NO3—)=c(NH4+)>c(OH—)= c(H+) ![]() Al—3e—= Al3+ 4OH- —4e-= 2H2O + O2↑ CO2
Al—3e—= Al3+ 4OH- —4e-= 2H2O + O2↑ CO2
【解析】
A是一种能使红色石蕊试液变蓝的气体,则A为NH3;甲为淡黄色固体化合物,应为Na2O2,用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成,说明A应为NH3,G为HNO3,则C为NO,B为H2O,E为NO2,乙在G的浓溶液中发生钝化,应为Al,生成F为NaAlO2,根据物质的性质结合题目的要求可解答该题。
(1)由以上分析可知甲为淡黄色固体化合物,应为Na2O2,为离子化合物,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成,说明A应为NH3,G为HNO3,则B为H2O,E为NO2 ,C为NO,反应Ⅰ为氨气的催化氧化反应,反应的化学方程式为4NH3+5O2![]() 4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(3)A为NH3,G为HNO3,溶液混合后存在电荷守恒:c(NO3-)+c(OH-)=c(NH4+)+c(H+),因为溶液显中性,则c(OH-)=c(H+)、c(NO3-)=c(NH4+),中性溶液中c(OH-)、c(H+)较小,则c(NO3-)=c(NH4+)>c(OH-)=c(H+);反应后剩余n(NH3H2O)=(a-b)mol,n(NH4+)=n(NO3-)=bmol,c(OH-)=10-7mol/L,则k=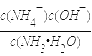 =
=![]() =
= ![]() (假定混合后溶液的体积为V),故答案为:c(NO3-)=c(NH4+)>c(OH-)=c(H+);
(假定混合后溶液的体积为V),故答案为:c(NO3-)=c(NH4+)>c(OH-)=c(H+);![]() ;
;
(4)①电解池阳极为Al,发生了两个电极反应,其中一个反应生成一种无色气体,应生成O2,电极方程式分别为Al-3e-=Al3+、4OH-
故答案为:Al-3e-=Al3+;4OH--4e-=2H2O+O2↑;
②负极电极方程式为CH4-8e-+4CO32-=5CO2+2H2O,正极为2O2+4CO2+8e-=4CO32-,可循环利用的为CO2,故答案为:CO2。

 考前必练系列答案
考前必练系列答案