题目内容
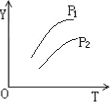
【题目】对于密闭容器中的可逆反应:4L(g)![]() 2M(g)+N(g) △H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示。图中y轴是指
2M(g)+N(g) △H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示。图中y轴是指
A. 气体混合物的平均相对分子质量 B. 气体混合物的总物质的量浓度
C. L在气体混合物的体积分数 D. 气体混合物的密度
【答案】A
【解析】试题分析:根据反应的方程式可知,该反应是体积减小的吸热的可逆反应,因此升高温度或增大压强平衡向正反应方向移动。根据图像可知随着温度升高和压强的增大,Y逐渐增大。A、混合气的平均相对分子质量等于混合气的质量与混合气总物质的量的比值,升高温度或增大压强平衡向正反应方向移动,在反应过程中混合气质量不变,但混合气的物质的量减小,因此气体混合物的平均相对分子质量逐渐增大,A正确;B、升高温度或增大压强平衡向正反应方向移动,在反应过程中混合气的物质的量减小,因此气体混合物的总物质的量浓度逐渐减小,B不正确;C、升高温度或增大压强平衡向正反应方向移动,所以L在气体混合物的体积分数减小,C不正确;D、升高温度或增大压强平衡向正反应方向移动,在反应过程中混合气质量和容器容积均不变,因此气体混合物的密度始终不变,D不正确,答案选A。

练习册系列答案
相关题目