题目内容
某无色溶液中只可能溶有NH4+、K+、Al3+、Mg2+、HCO3-、Cl-、I-、MnO4-、SO42-等离子中的几种离子。为分析其组成,现进行如下实验:
①取10mL该溶液于试管中滴加足量的Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲。
②取上述反应后的滤液,加入AgNO3溶液未见沉淀产生。
③另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加入NaOH的物质的量为0.03mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,换算成标况下为0.224L(假设丙全部逸出),最后沉淀完全溶解。
则下列说法正确的是
| A.仅由实验①可推出肯定含有SO42-,不含Cl- |
| B.该无色溶液肯定含有NH4+、K+、Al3+、SO42- |
| C.该无色溶液肯定不含K+、Mg2+、HCO3-、Cl-、MnO4-、I- |
| D.不能确定该无色溶液是否含有K+ |
D
解析试题分析;①可知该溶液中含有SO42-但是单单从①中 确定该溶液是否含有Cl-所以A选项是错误的。钾离子在整个反应中不能确定是否含有钾离子所以BC选项是错误的。所以答案选D
考点:考查离子反应的相关知识点

下列反应的离子方程式正确的是
| A.碳酸钙与稀硝酸反应: CaCO3+2H+= Ca2++ CO2↑+H2O |
| B.金属钠与水反应: 2Na +2H2O =2Na+ +2OH-+ H2↑ |
| C.铁溶于稀硫酸中: 2Fe+6H+= 2Fe3++3H2↑ |
| D.氢氧化钡溶液中滴加稀硫酸:Ba2+ + SO42-=BaSO4↓ |
下列物质中,属于强电解质的是
A.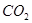 | B.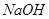 溶液 溶液 | C. | D.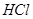 |
下列各组离子或分子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是 ( )
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
| A | NH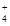 、Fe2+、SO 、Fe2+、SO | 少量Ba(OH)2溶液 | 2NH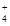 +SO +SO +Ba2++2OH-===BaSO4↓+2NH3·H2O +Ba2++2OH-===BaSO4↓+2NH3·H2O |
| B | Mg2+、HCO 、Cl- 、Cl- | 过量NaOH溶液 | Mg2++2HCO +4OH-===2H2O+Mg(OH)2↓+2CO +4OH-===2H2O+Mg(OH)2↓+2CO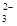 |
| C | K+、NH3·H2O、CO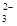 | 通入少量CO2 | 2OH-+CO2===CO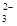 +H2O +H2O |
| D | Fe2+、NO 、HSO 、HSO | NaHSO4溶液 | HSO +H+===SO2↑+H2O +H+===SO2↑+H2O |
在H2SO4、K2SO4、Al2 (SO4)3和明矾[KAl(SO4)2·12H2O]的混合溶液中,H+的浓度为0.2mol/L,SO42-的浓度为0.5mol/L,当加入等体积0.6mol/L KOH溶液时,生成的沉淀恰好完全溶解。则反应后溶液中K+的浓度约为
| A.0.225mol/L | B.0.25mol/L | C.0.45mol/L | D.0.55mol/L |
铜粉加入稀盐酸中,加热无现象,这时加入一种盐则铜粉溶解而溶液变蓝,同时有气体放出,这种盐是
| A.NaCI | B.KNO3 | C.FeCl2 | D.Fe2(SO4)3 |
对于电解质溶液,下列说法正确的是
| A.甲基橙显黄色的溶液中,不可能有: Mg2+、K+、SO42- 、NO3- |
| B.无色溶液中还大量含有 :Al3+、 K+、 SO32- 、ClO- |
| C.Fe(OH)3溶于氢碘酸发生的反应为:Fe(OH)3+3H+= Fe3++3H2O |
| D.在稀氨水中通入过量CO2发生的反应为:NH3·H2O+CO2= NH4++HCO3- |
已知2MOyx-+5S2-+16H+=2M2+ +5S↓+ 8H2O,则下列选项正确的是
| A.x=2 | B.氧化产物和还原产物的比为2:5 |
| C.生成4mol H2O转移10mol电子 | D.MOyx-中的M的化合价为+7 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中( )
| A.至少存在5种离子 | B.Cl-一定存在,且c(Cl?)≥0.4mol/L |
| C.SO42-、NH4+、一定存在,Cl-可能不存在 | D.CO32-、Al3+一定不存在,K+可能存在 |