题目内容
【题目】织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体。25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出)。下列说法不正确的是( )
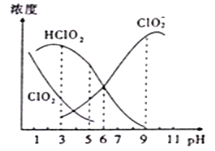
A.25℃时, ClO2-的水解平衡常数Ka=10-6
B.在pH约为4.0~4.5范围内使用该漂白剂较好
C.25℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:
c(HClO2)+c(H+)+c(Na+)=c(ClO2-)+2c(OH-)
D.当pH=5时往NaClO2溶液中滴入稀氢氧化钠溶液,溶液中主要反应的离子方程式是:HClO2+OH-=H2O+ClO2-
【答案】C
【解析】A.由图可知,当溶液的pH=6时,溶液中c(ClO2-)=c(HClO2),HClO2的电离平衡常数K= ![]() =10-6,故A正确;
=10-6,故A正确;
B.HClO2是漂白织物的有效成分,ClO2是有毒气体,要使漂白剂的漂白性强,即HClO2的含量高,又要使ClO2浓度较小,根据图象知,pH过小,ClO2含量较大,pH过大,HClO2的含量较低,当溶液的pH为4.0~4.5时二者兼顾,即为使用该漂白剂的最佳pH,应该是4-5,故正确;
C.依据电中性原则得出:c(H+)+c(Na+)=c(ClO2-)+c(OH-) ①,依据物料守恒得出:2c(Na+)=c(ClO2-)+c(HClO2) ②,联立①②消去钠离子:c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-),故C错误;
D. pH=5时,溶液中主要是HClO2,往NaClO2溶液中滴入稀氢氧化钠溶液,溶液中主要反应的离子方程式是:HClO2+OH-=H2O+ClO2-,正确。

【题目】下列分离或提纯有机物的方法正确的是( )
选项 | 待提纯物质 | 杂质 | 除杂试剂及主要操作方法 |
A | 乙烷 | 乙烯 | 酸性 KMnO4溶液, 洗气 |
B | 溴苯 | 溴 | NaOH 溶液,分液 |
C | 乙酸 | 乙醇 | 金属钠,蒸馏 |
D | 乙醇 | 水 | 生石灰,过滤 |
A. A B. B C. C D. D
