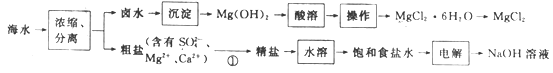
��Ŀ����
����Ŀ��ij��ѧ��ȤС����ʵ������ȡƯ�ۣ���̽��������ʯ���鷴Ӧ�������Ͳ��
��֪���ٶ���������Ũ���ᷴӦ���Ʊ�������ͬʱ����MnCl2
�������ͼ�ķ�ӦΪ���ȷ�Ӧ���¶Ƚϸ�ʱ�������ͼ�ܷ������·�Ӧ��3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
����ȤС�����������ʵ��װ�ã�����ʵ�顣
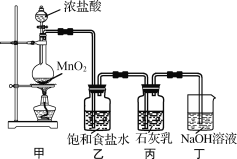
��ش��������⣺
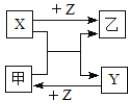
��1���ټ�װ�������Ʊ���������װ�õ�������__��
��ʵ����������NaOH��Һ���մ�Ũ�����MnO2��Ӧ��ϵ�е��������塣�������¶Ȳ�ͬʱ�����ɵIJ��������NaClO��NaClO3��NaCl�е����ֻ����֡�����˵������ȷ����_��������ĸ��
A��������ΪNaClO3��NaCl����μӷ�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ1��5
B��������ΪNaClO��NaCl�������պ����Һ��n(NaClO)=n(NaCl)
C��������ΪNaClO��NaClO3��NaCl����NaOH��Cl2���Ӧ�����ʵ���֮��Ϊ2��1
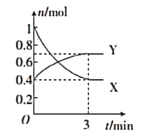
��2��С���Ա���֣�������Ca(ClO)2����������С������ֵ���������ۺ���Ϊ�������ԭ���Dz�������δ��ʯ���鷴Ӧ���ݳ����Լ��¶����ߡ�Ϊ��̽����Ӧ�����Բ����Ӱ�죬������ȡһ������ʯ���飬�������ٵ�ͨ�������������ó���Ca(ClO)2��Ca(ClO3)2�������ʵ����ʵ�����n���뷴Ӧʱ�䣨t���Ĺ�ϵ���ߣ����Ա�ʾΪ��ͼ(������������ˮ�ķ�Ӧ)��
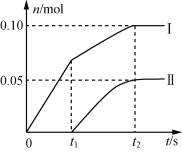
��ͼ������II��ʾ__(�����ʵĻ�ѧʽ)�����ʵ����淴Ӧʱ��仯�Ĺ�ϵ��
����ȡʯ�����к���Ca(OH)2�����ʵ���Ϊ__mol��
���𰸡���ȥ�����л��е��Ȼ��� AB Ca(ClO3)2 0.5
��������
��1��������Ũ������ȡ�������г�����HCl���壬HClҲ����Ca(OH)2������Ӧ��ʹ����Ч�ɷֺ������ͣ���Ҫ���ӣ���װ�õ����þ������ڳ�ȥ�����е�HCl�����dz�ȥ�����л��е��Ȼ��⣻
��A��������ΪNaClO3��NaCl����ѧ����ʽ6NaOH+3Cl2=5NaCl+NaClO3+3H2O�����ݷ���ʽ��֪���������ϼ����ߵõ�NaClO3��ֻ��0.5mol�����������ϼ۽��͵õ�NaCl��2.5mol������������ԭ����Ϊ�����������ʵ���֮��Ϊ2.5��0.5=5��1��A�����
B��Ũ�����MnO2��Ӧ��ϵ�е����������к�������HCl��������NaOH��Ӧ����NaClO��NaCl�ķ���ʽ2NaOH+Cl2=NaCl+NaClO+H2O��NaClO��NaCl�����ʵ���֮��Ϊ1��1������HClҲ����NaOH��Ӧ����NaCl����˱���������1��1��B�����
C��������NaCl��NaClO����NaClO3�У�Na��Cl�ı�����Ϊ1��1��1mol�����к���2mol Clԭ�ӣ�����ԭ���غ㣬��NaOH��Cl2�ı���Ϊ1��2��C����ȷ��
��ΪAB��
(2)�ٷ�Ӧ�տ�ʼ��ʱ��������Ca(OH)2����Ca(ClO)2����Һ���¶Ȳ����ߣ���Ȼ��Ӧ���ȣ��¶������ߣ�������Ca(OH)2��Ӧ����Ca(ClO3)2���������ߢ��ʾ����Ca(ClO3)2�����ʵ����淴Ӧʱ��仯�Ĺ�ϵ����ΪCa(ClO3)2���ڸ���ͼ���֪��Ca(ClO)2�����ʵ���Ϊ0.1mol��Ca(ClO3)2�����ʵ���Ϊ0.05mol�����ݻ�ѧ����ʽ2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O��6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O�����ܹ�����Ca(OH)2�����ʵ���Ϊ0.1mol��2+0.05mol��6=0.5mol����Ϊ0.5��