题目内容
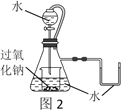
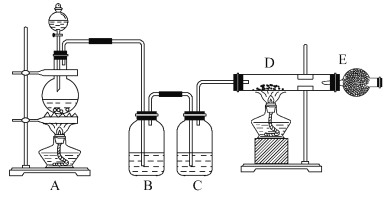
【题目】下图所示是制取无水氯化铜的实验装置图,在A装置中将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中,烧瓶中发生反应的原理为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
请回答下列问题:
(1)装置中盛放浓盐酸的仪器名称为_______。
(2)B瓶中试剂的作用是除去氯气中含有的氯化氢气体,C瓶中试剂的作用是______。
(3)玻璃管D中的反应方程式是________________。
【答案】分液漏斗 干燥氯气(或写为除去氯气中的水蒸气) Cu+Cl2![]() CuCl2
CuCl2
【解析】
在装置A中MnO2与浓盐酸发生反应制取Cl2,浓盐酸具有挥发性,使Cl2中含有杂质HCl、水蒸气,通过装置B中的饱和NaCl溶液除去杂质HCl,然后通过装置C的浓硫酸干燥氯气,在装置D中干燥纯净的Cl2与Cu发生反应产生CuCl2。
(1)液体反应物浓盐酸盛放在分液漏斗中,固体MnO2在烧瓶中,将浓盐酸滴入烧瓶中,在加热条件下反应产生Cl2,反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,根据装置可知盛装浓盐酸的仪器是分液漏斗;
MnCl2+Cl2↑+2H2O,根据装置可知盛装浓盐酸的仪器是分液漏斗;
(2)由于浓盐酸具有挥发性,因此制取得到的氯气中含有杂质HCl、水蒸气,B瓶中试剂的作用是除去氯气中含有的杂质HCl气体,C瓶中试剂是浓硫酸,作用是干燥氯气;
(3)在玻璃管D中的Cu与Cl2反应产生CuCl2,反应的方程式是Cu+Cl2![]() CuCl2。
CuCl2。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目