题目内容
【题目】碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1) 甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l)△H1=-1214kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2=-566 kJ/mol
则表示甲烷燃烧热的热化学方程式____________________________________。
(2) 将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其负极电极反应式是:_____________________________。
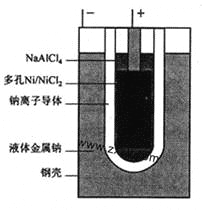
(3)某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是______(填序号)

A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H++ 2e-= H2↑
(4)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g)===CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
H2O | CO | CO2 | |||
1 | 650 | 2 | 4 | 1.6 | 5 |
2 | 900 | 1 | 2 | 0.4 | 3 |
3 | 900 | 1 | 2 | 0.4 | 1 |
①实验
②实验3跟实验2相比,改变的条件可能是_________________(答一种情况即可)。
【答案】CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=-890KJmol-1 CH4-8e-+ 10 OH-=CO32-+ 7H2O B、D 0.16mol/(L·min) 使用催化剂 增大压强(任答一种)
【解析】
(1)根据盖斯定律,由已知热化学方乘以适当的系数进行加减构造目标热化学方程式,反应热也乘以相应的系数并进行相应的加减,据此计算;
(2)①根据CH4和O2构成燃料电池,甲烷在负极发生氧化反应,碱性环境下生成CO32-;
(3)A、B端析出氢气可驱赶原溶液中溶解的少量氧气;
B、电解液选用NaCl溶液不影响实验,因为阳极是铁失电子生成亚铁离子,溶液中的阴离子不放电;
C、阳极应该用铁电极,阴极用惰性电极亦可;
D、B电极反应是阴极氢离子放电生成氢气;
(4)①根据图表数据,CO2的浓度增加0.8mol/L,所以氢气浓度也增加0.8mol/L,v (H2)= ![]() 进行计算;
进行计算;
②实验3跟实验2相比,温度相同,浓度相同,但实验3达到平衡所用时间少,反应速率更大,平衡不移动,可以使用催化剂或增大压强等。
(1)甲烷完全燃烧生成二氧化碳气体和液态水,所以甲烷燃烧热的热化学方程式中甲烷的物质的量是1mol,将①②相加除以2可得:CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) △H1=-890KJmol-1;
CO2(g)+2H2O(l) △H1=-890KJmol-1;
答案是:CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) △H1=-890KJ.mol-1
CO2(g)+2H2O(l) △H1=-890KJ.mol-1
(2)负极发生氧化反应,所以甲烷在负极发生氧化反应,结合电解质溶液,负极的电极反应式为CH4- 8e-+ 10 OH-![]() CO32-+ 7H2O;
CO32-+ 7H2O;
(3)A、电解过程中两极分别是H+和Fe放电生成氢气和亚铁离子,所以两极哪端都可以生成氢气,a不一定为正极,b不一定为负极,但a为正极,b为负极,效果较好,错误;B、在装置中铁一定作阳极,所以氯化钠溶液是电解质溶液,不影响阳极Fe放电生成亚铁离子,阴极H+放电生成氢气,正确;
C、装置中铁一定作阳极,阴极可以是铁,也可以是其他惰性电极,错误;
D、阴极H+放电生成氢气,正确;
答案选BD。
(4)①实验1中,CO2的浓度增加0.8mol/L,所以氢气浓度也增加0.8mol/L,v (H2)= ![]() =0.16mol/(L·min);
=0.16mol/(L·min);
②实验3跟实验2相比,到达平衡时间缩短,说明反应速率加快,反应温度、各物质的物质的量均未变,所以可能是使用了催化剂或增大压强。

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案【题目】下列有关实验操作、现象和结论都正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向稀硝酸中加入过量的铁粉充分反应后,滴入KSCN溶液 | 溶液变为血红色 |
|
B | 向盛有某溶液的试管中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸颜色无明显变化 | 原溶液中无 |
C | 向淀粉溶液中加入稀硫酸,加热,冷却后加入新制 | 未见红色沉淀 | 淀粉未发生水解 |
D | 向含有酚酞的 | 溶液红色变浅 | 证明 |
A.AB.BC.CD.D