题目内容
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,部分元素在周期表中的位置关系如右图所示.其中X是周期表中原子半径最小的元素,Q与X同主族;Z的最外层电子数是次外层的3倍.
Y | Z | ||
R |
请回答下列问题:
(1)写出Y元素的名称: , Q的原子结构示意图;R在周期表中的位置为 .
(2)Q2Z电子式为: , Q2Z2含的化学键类型为: .
(3)R、Z分别形成简单离子的半径大小:(离子符号表示)
(4)Y的氢化物与其最高价氧化物对应的水化物反应的化学方程式为: .
【答案】
(1)氮;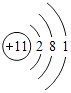 ;第三周期ⅢA族
;第三周期ⅢA族
(2)![]() ;离子键、共价键;
;离子键、共价键;
(3)Al3+<O2﹣
(4)NH3+HNO3═NH4NO3
【解析】解:X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,部分元素在周期表中的位置关系如右图所示,则Y、Z位于第二周期、R位于第三周期;X是周期表中原子半径最小的元素,则X为H元素;Z的最外层电子数是次外层的3倍,最外层最多容纳8个电子,则Z含有2个电子层,最外层含有6个电子,为O元素;根据各元素在周期表中的相对位置可知Y为N、R为Al元素;Q与X同主族,Q的原子序数大于O,则Q为Na元素,(1)Y为N元素,名称为氮;Q为Na元素,其原子序数为11,其原子结构示意图: 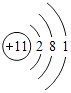 ;R为Al元素,原子序数为13,位于周期表中第三周期ⅢA族, 所以答案是:氮;
;R为Al元素,原子序数为13,位于周期表中第三周期ⅢA族, 所以答案是:氮; 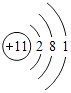 ;第三周期ⅢA族;(2)Q2Z为Na2O,氧化钠为离子化合物,其电子式为:
;第三周期ⅢA族;(2)Q2Z为Na2O,氧化钠为离子化合物,其电子式为: ![]() ;Q2Z2为Na2O2 , 过氧化钠为离子化合物,其电子式为
;Q2Z2为Na2O2 , 过氧化钠为离子化合物,其电子式为 ![]() ,化学式中含有离子键和共价键,
,化学式中含有离子键和共价键,
所以答案是: ![]() ;离子键、共价键;(3)R、Z分别形成简单离子分别为Al3+、O2﹣ , 两种离子都含有2个电子层,核电荷数越大离子半径越小,则离子半径大小为:Al3+<O2﹣ ,
;离子键、共价键;(3)R、Z分别形成简单离子分别为Al3+、O2﹣ , 两种离子都含有2个电子层,核电荷数越大离子半径越小,则离子半径大小为:Al3+<O2﹣ ,
所以答案是:Al3+<O2﹣;(4)Y为N元素,对应的氢化物为氨气,对应的最高价氧化物的水化物为硝酸,二者发生反应为:NH3+HNO3═NH4NO3 ,
所以答案是:NH3+HNO3═NH4NO3 .



