题目内容
19.实验室用氯酸钾和二氧化锰制取氧气,加热一段时间后剩余固体混合物10g,继续加热至完全反应后固体变为9.04g,再将固体加水充分溶解、过滤、干燥得到1.59g黑色固体.求10g剩余固体混合物中氯元素的质量分数为( )| A. | 7.1% | B. | 35.5% | C. | 28.4% | D. | 42.6% |
分析 最终得到的1.59g黑色固体为二氧化锰,则完全反应后,所得氯化钾的质量为:9.04g-1.59g=7.45g,根据氯化钾的化学式组成可以计算出氯元素的质量;氯元素的质量在反应前后没有发生变化,据此可以计算出在10g剩余固体混合物中氯元素的质量分数.
解答 解:根据题意可知,1.59g黑色固体为二氧化锰,则完全反应后,所得氯化钾的质量为:9.04g-1.59g=7.45g,
则其中含氯元素的质量为:7.45g×($\frac{35.5}{74.5}$×100%)=3.55g,
氯元素的质量在反应前后没有发生变化,所以在10g剩余固体混合物中氯元素的质量分数为:$\frac{3.55g}{10g}$×100%=35.5%,
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,明确反应后固体组成为解答关键,注意掌握质量守恒定律在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
10.如图为周期表的一部分,所有元素都是主族元素,不正确的是( )
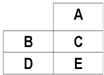

| A. | E的核电荷数大于B | |
| B. | A、C若为非金属,则对应氢化物的稳定性:A>C | |
| C. | B、D若为金属,其最高价氧化物对应水化物碱性:D>B | |
| D. | A一定是非金属元素 |
7.自来水厂生产自来水的工艺流程示意图如图所示

“加氯”是指加入含有氯元素的物质,该物质可以是( )

“加氯”是指加入含有氯元素的物质,该物质可以是( )
| A. | 氯气 | B. | ClO2 | C. | NaCl | D. | NaClO3 |
14.国际互联网上报道:“目前世界上有近20亿人患有缺铁性贫血”.我国政府 即将启动“酱油补铁工程”.这里的铁指( )
| A. | 铁元素 | B. | 铁单质 | C. | 四氧化三铁 | D. | 三氧化二铁 |
8.给3mL液体加热,需使用的仪器有( )
①试管 ②烧杯 ③试管夹 ④酒精灯⑤蒸发皿 ⑥石棉网 ⑦铁架台(带铁圈)
①试管 ②烧杯 ③试管夹 ④酒精灯⑤蒸发皿 ⑥石棉网 ⑦铁架台(带铁圈)
| A. | ①③④⑤ | B. | ②④⑥ | C. | ①③④ | D. | ②④⑥⑦ |
9.某3种简单原子的原子核结构可用下图形象地表示(?表示质子,○表示中子):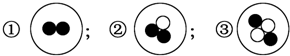
则有关这三种原子的叙述中正确的是( )

则有关这三种原子的叙述中正确的是( )
| A. | 它们是不同元素的原子 | B. | 它们单质的化学性质相同 | ||
| C. | 这三种原子具有不同的核电荷数 | D. | 这三种原子具有相同的质量数 |
