题目内容
3.下列说法中,正确的是( )| A. | 气体摩尔体积为22.4L•mol-1 | |
| B. | 1molH2的质量是2g,它所占的体积是22.4L | |
| C. | 1mol水中含有2mol氢和1mol氧 | |
| D. | 在标准状况下,1mol任何气体所占的体积都约为22.4L |
分析 A.不是标准状况下,气体摩尔体积不一定是22.4L/mol;
B.物质的量一定时,温度、压强会影响气体的体积;
C.使用物质的量应指明具体的物质或微粒;
D.在标准状况下,气体摩尔体积约是22.4K/mol,1mol任何气体所占的体积都约为22.4L.
解答 解:A.温度、压强影响气体摩尔体积,不是标准状况下,气体摩尔体积不一定是22.4L/mol,故A错误;
B.1molH2的质量是1mol×2g/mol=2g,物质的量一定时,温度、压强会影响气体的体积,其只有的体积不一定是22.4L,故B错误;
C.1mol氢、1mol氧指代不明确,使用物质的量应指明具体的物质或微粒,故C错误;
D.在标准状况下,气体摩尔体积约是22.4K/mol,1mol任何气体所占的体积都约为22.4L,故D正确,
故选:D.
点评 本题考查气体摩尔体积,难度不大,注意气体摩尔体积的属于条件与对象,根据PV=nRT理解温度、压强对气体摩尔体积的影响.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
14.如图所示的反应过程中,关于乙烯所发生的反应类型的叙述正确的是( )
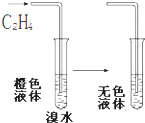

| A. | 氧化反应 | B. | 还原反应 | C. | 取代反应 | D. | 加成反应 |
11.某无色溶液中存在大量的NH4+、Ba2+、Cl-,该溶液中还可能大量存在的是( )
| A. | SO42一 | B. | Cu2+ | C. | Ag+ | D. | NO${\;}_{3}^{-}$ |
18.下列说法正确的是( )
| A. | 甲烷的燃烧热为 890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol | |
| B. | 500℃、30 MPa 下,将 0.5 mol N2 和 1.5 mol H2 置于密闭的容器中充分反应生成 NH3(g),放热 19.3 kJ,其热化学方程式为 N2(g)+3H2(g)?2NH2(g)△H=-38.6 kJ•mol | |
| C. | 一定条件下,反应 N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol降低温度将向正反应方向移动 | |
| D. | 已知 2C(s)+2O2(g)═2CO2(g)△H12C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
8.下列铁的化合物可以分别通过化合反应、置换反应、复分解反应生成的是( )
| A. | FeCl2 | B. | Fe3O4 | C. | Fe(OH)3 | D. | Fe2(SO4)3 |
15. 常温下,取pH=2的 HA溶液与HB溶液各1mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示.下列叙述正确的是( )
常温下,取pH=2的 HA溶液与HB溶液各1mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示.下列叙述正确的是( )
 常温下,取pH=2的 HA溶液与HB溶液各1mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示.下列叙述正确的是( )
常温下,取pH=2的 HA溶液与HB溶液各1mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示.下列叙述正确的是( )| A. | 稀释前,c(HB)>c(HA)=0.01 mol•L-1 | |
| B. | HB的电离方程式为HB=H++B- | |
| C. | NaA的水溶液中,离子浓度大小为:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| D. | NaA、NaB的混合溶液中:2c(Na+)=c(A-)+c(B-)+c(HB) |
12.几种短周期元素的原子半径及某些化合价见下表.分析判断下列说法正确的是( )
| 元素 代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半 径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A. | G元素的单质不存在同素异形体 | |
| B. | I在DB2中燃烧生成两种化合物 | |
| C. | A的单质能将E单质从HE3的溶液中置换出来 | |
| D. | A、H、J的离子半径由大到小顺序是A>J>H |