题目内容
【题目】如图所示,装置连接好后,电流计指针发生了偏转,下列说法中正确的是
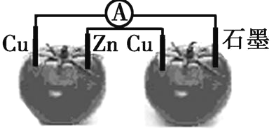
A.两个番茄及相关电极均构成了原电池
B.锌是负极
C.电子移动:锌→铜(右)→番茄→石墨→铜(左)
D.两个铜片上均发生氧化反应
【答案】B
【解析】
左侧为铜-锌水果电池,发生的是原电池反应,锌作负极、发生氧化反应,铜作正极、发生还原反应;右侧装置是电解池,铜作电解池的阴极、发生还原反应,石墨作电解池的阳极、发生氧化反应,据此分析解答。
A、左侧番茄及相关电极构成了原电池,右侧番茄及相关电极构成了电解池,故A错误;
B、铜-锌-番茄原电池中,Zn较活泼,作负极,故B正确;
C、左侧装置为原电池,锌作负极、铜作正极;右侧装置为电解池,铜作阴极、石墨作阳极,电子移动:锌→铜(右),石墨→铜(左),电子不能在番茄中移动,故C错误;
D、左侧装置为原电池,原电池中铜为正极,电极上氢离子得电子发生还原反应,右侧装置是电解池,铜为阴极,阴极上阳离子得电子发生还原反应,故D错误;
故选B。

练习册系列答案
相关题目