题目内容
13.下列说法正确的是( )| A. | KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | |
| B. | HClO是弱酸,所以NaClO是弱电解质 | |
| C. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| D. | BaSO4 和NaHCO3都是强电解质 |
分析 A.电解质必须是本身能够电离;
B.次氯酸钠为盐,在水溶液或者熔融状态下能够完全电离;
C.含有离子键的化合物属于离子化合物,只含共价键的化合物属于共价化合物;
D.能够完全电离的电解质是强电解质.
解答 解:A.三氧化硫溶于水导电是因为生成电解质硫酸,三氧化硫本身不能电离,属于非电解质,故A错误;
B.次氯酸钠为盐,在水溶液或者熔融状态下能够完全电离,属于强电解质,故B错误;
C.氯化氢只含有共价键属于共价化合物,故C错误;
D.硫酸钡在熔融状态下、碳酸氢钠溶于水都能够完全电离,属于强电解质,故D正确;
故选:D.
点评 本题考查了电解质、非电解质、强电解质、弱电解质,明确概念是解题关键,注意电解质强弱区分依据是电离程度,题目难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
1.下列离子方程式或热化学方程式正确的是( )
| A. | 在不同温度下,以相同浓度相同体积的Na2S2O3与H2SO4反应来探究温度对化学反应速率的影响:3S2O32-+2SO42+10H+═6SO2↑+2S↓+5H2O | |
| B. | 酸性条件下,KI被O2氧化的离子方程式:4I-+O2+4H+═2I2+2H2O | |
| C. | 已知25℃、101kPa时,1molH2与溴蒸气完全反应生成气态HBr放出能量Q kJ,其热化学方程式为H2(g)+Br2(g)═2HBr(g)△H=-2Q kJ•mol-1 | |
| D. | 表示中和热的热化学方程式:2HCl(aq)+Ba(OH)2(aq)═BaCl2(aq)+2H2O(l)△H=-114.6 |
8.一般情况下胶体稳定,胶体微粒不易聚集,主要原因是( )
| A. | 胶体粒子因吸附带电荷离子而带同种电荷 | |
| B. | 胶体有布朗运动 | |
| C. | 胶体粒子直径在1~100nm之间,粒子小,不受重力作用 | |
| D. | 胶体有丁达尔现象 |
18.下列化学用语表达不正确的是( )
| A. | 图为丙烷的球棍模型: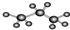 | B. | 丙烯的结构简式为:CH3CHCH2 | ||
| C. | 某有机物的名称是:2,3二甲基戊烷 | D. | 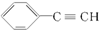 的最简式为:C4H3 的最简式为:C4H3 |
2.下列对进行下列有关判断中,正确的是( )
| A. | 加入足量的CaCl2溶液,产生了白色沉淀,则溶液中一定含有大量的CO32- | |
| B. | NaCl溶液与Na2CO3固体灼烧时火焰颜色相同 | |
| C. | 通过灼热的CuO,能使固体由黑变红的气体一定是H2 | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
3.化学来自于生活,用于生活,下表是生活中常用物质溶液的PH值及主要成分的化学式:
试回答:
(1)将上表①~⑤中主要成分进行分类(填序号,下同):属于酸的是①;属于碱的是④;属于盐的是⑤;属于有机物的是①②③.
(2)当有人被蚊虫(释放一种酸性物质)叮咬后,为减轻疼痛,可在伤处涂④⑤.
(3)用久的铝壶内有水垢(主要成分为CaCO3、Mg(OH)2可用①少量多次清除.
| 编号 | ① | ② | ③ | ④ | ⑤ |
| 名称 | 食醋 | 白酒 | 白糖水 | 石灰水 | 纯碱溶液 |
| 主要成分 | CH3COOH | C2H5OH | C12H22O11 | Ca(OH)2 | Na2CO3 |
| 溶液PH | 3 | 7 | 7 | 11 | 10 |
(1)将上表①~⑤中主要成分进行分类(填序号,下同):属于酸的是①;属于碱的是④;属于盐的是⑤;属于有机物的是①②③.
(2)当有人被蚊虫(释放一种酸性物质)叮咬后,为减轻疼痛,可在伤处涂④⑤.
(3)用久的铝壶内有水垢(主要成分为CaCO3、Mg(OH)2可用①少量多次清除.

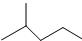 表示的分子式C6H14;名称是2-甲基戊烷,核磁共振氢谱中有5组峰.
表示的分子式C6H14;名称是2-甲基戊烷,核磁共振氢谱中有5组峰.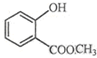 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.