题目内容
5.燃烧0.1mol某烃可得到0.4mol二氧化碳,在催化剂作用下,0.1mol该烃能跟0.2mol氢气发生加成反应,则此烃可能是( )| A. | 1-丁烯 | B. | 2-丁烯 | C. | 1,3-丁二烯 | D. | 1-丁炔 |
分析 由碳原子守恒可知该烃中含有4个C原子,0.1mol该烃能跟0.2mol氢气发生加成反应,则该烃含有1个C≡C三键或2个C=C双键,据此进行解答.
解答 解:燃烧0.1mol某烃可得到0.4mol二氧化碳,由碳原子守恒可知该烃中含有C原子数为$\frac{0.4mol}{0.1mol}$=4,0.1mol该烃能跟0.2mol氢气发生加成反应,则该烃含有1个C≡C三键或2个C=C双键,选项中1,3-丁二烯与1-丁炔符合,故选:CD.
点评 本题考查有机物分子式的确定,难度不大,确定含有的官能团为解答关键,注意掌握原子守恒在确定有机物分子式中的应用.

练习册系列答案
相关题目
15.将碘水中的碘萃取出来的实验中,下列说法错误的是( )
| A. | 分液漏斗使用前要检查它是否漏水 | |
| B. | 要求萃取剂既不溶于水,且比水更容易使碘溶解 | |
| C. | 分液漏斗注入碘水和萃取剂,反复倒转并用力振荡后,不必静置,应立即分液 | |
| D. | 分液时,下层液体应从下口放出,上层液体应从上口倒出 |
13.已知氢气的燃烧热为285.8kJ/mol,CO的燃烧热为282.8kJ/mol;现有H2和CO组成的混合气体56.0L(标准状况),经充分燃烧后,放出总热量为710.0kJ,并生成液态水.下列说法正确的是( )
| A. | CO燃烧的热化学方程式为:2CO(g)+O2(g)=2CO2(g)△H=+285.8kJ/mol | |
| B. | H2燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ/mol | |
| C. | 燃烧前混合气体中H2的体积分数为40% | |
| D. | 燃烧后的产物全部与足量的过氧化钠作用可产生1.25mol氧气 |
20.下列有关气态氢化物某些性质的归纳正确的是( )
①H2S、H2Se在水中的溶解度较小,CH4、SiH4、C2H2不溶于水;
②HF最稳定、SiH4较稳定;
③NH3、H2Se、H2To能在纯氧中燃烧,常温下SiH4能自燃;
④H2S、HI还原性娇弱,NH3、HBr还原性较强;
⑤H2S、HF溶液的导电性较弱.
①H2S、H2Se在水中的溶解度较小,CH4、SiH4、C2H2不溶于水;
②HF最稳定、SiH4较稳定;
③NH3、H2Se、H2To能在纯氧中燃烧,常温下SiH4能自燃;
④H2S、HI还原性娇弱,NH3、HBr还原性较强;
⑤H2S、HF溶液的导电性较弱.
| A. | ①③ | B. | ③④ | C. | ②④⑤ | D. | ①③⑤ |
5.甲、乙两种非金属:①甲比乙容易与氢气化合;②甲能与乙的阴离子发生置换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低.能说明甲比乙的非金属性强的是( )
| A. | 只有④ | B. | 只有⑤ | C. | ①②③④⑤ | D. | ①②③ |
12.室温下,甲、乙两烧杯均盛有5mL pH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4.关于甲、乙烧杯中溶液的描述正确的是( )
| A. | 溶液的体积10V甲≤V乙 | |
| B. | 水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 | |
| C. | 若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 | |
| D. | 若分别与5 mL pH=11的NaOH溶液反应,所得溶液的pH:乙≤甲 |
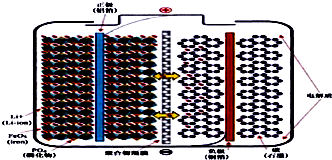 磷酸铁锂动力电池(LiFePO4电池)的内部结构如图所示.中间是聚合物的隔膜,它把正极与负极隔开,锂离子可以通过而电子不能通过.该电池的总反应式为:Li1-xFePO4+LixC6═C6+LiFePO4
磷酸铁锂动力电池(LiFePO4电池)的内部结构如图所示.中间是聚合物的隔膜,它把正极与负极隔开,锂离子可以通过而电子不能通过.该电池的总反应式为:Li1-xFePO4+LixC6═C6+LiFePO4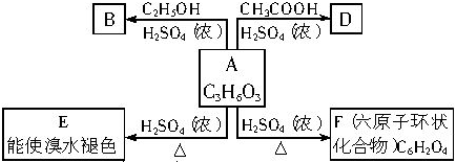
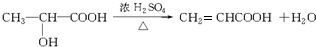 A→F
A→F