题目内容
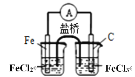
【题目】下列指定反应的离子方程式正确的是
A.用KIO3溶液氧化酸性溶液中的KI:5I-+ IO3- + 3H2O = 3I2 + 6OH-
B.醋酸溶液与水垢中的CaCO3反应:CaCO3 + 2H+ = Ca2+ + H2O + CO2![]()
C.Cu溶于稀HNO3:Cu + 2H+ + NO3- = Cu2+ + NO2↑+ H2O
D.Ca(HCO3)2溶液与足量NaOH溶液反应:2HCO3- + Ca2+ + 2OH-= CaCO3↓ + CO32-+ 2H2O
【答案】D
【解析】
A.KIO3氧化酸性溶液中的KI产物中不能生成氢氧根离子,反应的离子方程式为:5I-+ IO3- +6H+═3I2+3H2O,故A错误;
B. 醋酸溶液除水垢中的CaCO3反应的离子反应为CaCO3+2CH3COOH=Ca2++2CH3COO+H2O+CO2↑,故B错误;
C.Cu溶于稀HNO3生成硝酸铜、NO气体和水,正确的离子方程式为:3Cu +8H+ + 2NO3- = ═3Cu2++2NO↑+4H2O,故C错误;
D.Ca(HCO3)2溶液与足量NaOH溶液反应,离子方程式:2HCO3- + Ca2+ + 2OH-= CaCO3↓ + CO32-+ 2H2O故D正确;
答案选D。

练习册系列答案
相关题目