题目内容
某同学从报刊上了解到菠菜中富含可溶性草酸盐和碳酸盐,决定用实验验证这一事实并检测草酸盐含量。进一步查阅资料得知,草酸(H2C2O4)是酸性强于醋酸的二元有机酸,还是一种还原性较强的物质,如2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O,草酸钙(CaC2O4)不溶于水和醋酸,能溶于强酸:CaC2O4+2H+= H2C2O4+Ca2+。
(1)设计实验方案验证菠菜中含有草酸盐和碳酸盐,补充完成实验步骤、预期现象和结论。
限选试剂:1 mol·L-1 H2SO4、1 mol·L-1 HCl、0.1 mol·L-1 NaOH、1 mol·L-1 CaCl2、0.01 mol·L-1 KMnO4、澄清石灰水。
(2)要准确测定菠菜中草酸盐含量,请回答有关问题:
① 操作:取m g菠菜样品,将其中草酸盐转化为CaC2O4沉淀分离出来,用盐酸溶解后,将溶液转入_________中加水配制成100mL溶液。每次用_____________移取25.00mL该溶液,用0.0100mol·L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。
② 计算:菠菜中草酸盐(以C2O42-计)的质量分数为___________________。(只列式不计算。C2O42-的化学式量为88)
③ 讨论:用标准KMnO4溶液直接滴定菠菜研磨、浸泡、过滤得到的溶液,结果可能偏高,原因是 。
(1)设计实验方案验证菠菜中含有草酸盐和碳酸盐,补充完成实验步骤、预期现象和结论。
限选试剂:1 mol·L-1 H2SO4、1 mol·L-1 HCl、0.1 mol·L-1 NaOH、1 mol·L-1 CaCl2、0.01 mol·L-1 KMnO4、澄清石灰水。
| 实验步骤 | 预期现象和结论 |
| 步骤1:将菠菜研磨后,浸泡、过滤得到澄清待测溶液。 | |
| 步骤2:调节溶液至弱碱性,滴加足量CaCl2溶液。 | 出现白色沉淀,说明菠菜中可能含有草酸盐和碳酸盐。 |
| 步骤3:取步骤2的沉淀于试管中, | |
| 步骤4: | |
(2)要准确测定菠菜中草酸盐含量,请回答有关问题:
① 操作:取m g菠菜样品,将其中草酸盐转化为CaC2O4沉淀分离出来,用盐酸溶解后,将溶液转入_________中加水配制成100mL溶液。每次用_____________移取25.00mL该溶液,用0.0100mol·L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。
② 计算:菠菜中草酸盐(以C2O42-计)的质量分数为___________________。(只列式不计算。C2O42-的化学式量为88)
③ 讨论:用标准KMnO4溶液直接滴定菠菜研磨、浸泡、过滤得到的溶液,结果可能偏高,原因是 。
(16分)(1)(共8分)
(2)① 100mL容量瓶 酸式滴定管(2分,每种仪器1分)
②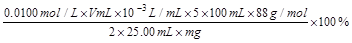 (其它合理表示方法也给分)(4分,算式中不带单位也给分,有效数字不准确扣1分)
(其它合理表示方法也给分)(4分,算式中不带单位也给分,有效数字不准确扣1分)
③ 菠菜中还含有其他还原性物质,能与KMnO4反应(2分)
| 实验步骤 | 预期现象和结论 |
| 步骤3:加入足量1 mol·L-1 HCl,将产生的气体通入足量澄清石灰水中。(2分) | 沉淀溶解,澄清石灰水变浑浊,说明菠菜中含有碳酸盐。(2分) |
| 步骤4: 向步骤3得到的溶液中滴加几滴0.01 mol·L-1 KMnO4。(2分) | 溶液紫红色褪去,说明菠菜中含有草酸盐。(2分) |
(2)① 100mL容量瓶 酸式滴定管(2分,每种仪器1分)
②
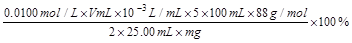 (其它合理表示方法也给分)(4分,算式中不带单位也给分,有效数字不准确扣1分)
(其它合理表示方法也给分)(4分,算式中不带单位也给分,有效数字不准确扣1分)③ 菠菜中还含有其他还原性物质,能与KMnO4反应(2分)
试题分析:(1)依题意,步骤2所得沉淀可能是碳酸钙,也可能是草酸钙,还可能是碳酸钙和草酸钙组成的混合物;由于草酸的酸性比醋酸强,醋酸的酸性比碳酸强,草酸钙不溶于水和醋酸,能溶于强酸,而碳酸钙不溶于水,能溶于醋酸,也能溶于强酸,因此向步骤2所得沉淀中加入足量1 mol·L-1 HCl,若沉淀完全溶解,且产生的气体通入足量澄清石灰水时,澄清石灰水变浑浊,说明沉淀中存在碳酸钙,证明菠菜中含有碳酸盐;由于草酸具有还原性,能使酸性高锰酸钾溶液褪色,即2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O,因此向步骤3所得上层清液中先滴入足量1 mol·L-1 H2SO4,再滴入几滴或少量0.01 mol·L-1 KMnO4,溶液紫红色褪去,说明菠菜中含有草酸盐;(2)①配置100mL一定物质的量浓度的溶液,称量、搅拌溶解后,应将溶液转移入100mL容量瓶中,洗涤之后定容;由于草酸溶液显酸性,所以选用酸式滴定管量取25.00mL草酸溶液;②由于n=c?V,则每次滴定时消耗标准溶液中KMnO4的物质的量为0.0100×V×10-3mol;由于2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O中草酸与高锰酸钾的系数之比等于物质的量之比,则每次滴定时待测溶液中H2C2O4的物质的量为0.0100×V×10-3×5/2mol;由于菠菜样品所配溶液的体积与滴定时待测溶液的体积之比为100/25.00,则菠菜样品所配溶液中H2C2O4的物质的量为0.0100×V×10-3×5/2×100/25.00mol;由于C2O42-~H2C2O4中草酸根离子与草酸的系数之比等于物质的量之比,则菠菜中C2O42-的物质的量为0.0100×V×10-3×5/2×100/25.00×1/1mol;由于草酸根离子的式量为88,m=n?M,则菠菜中C2O42-的质量为0.0100×V×10-3×5/2×100/25.00×1/1×88g;由于菠菜的质量为mg,则菠菜中C2O42-的质量分数为0.0100×V×10-3×5/2×100/25.00×1/1×88/m×100%;③菠菜中不仅草酸盐可以被酸性高锰酸钾溶液氧化,而且别的有机物(如维生素C等)也能被酸性高锰酸钾溶液氧化,因此用标准高锰酸钾溶液直接滴定菠菜研磨、浸泡、过滤得到的溶液,消耗酸性高锰酸钾溶液的体积偏大,因此测定结果偏高。

练习册系列答案
相关题目
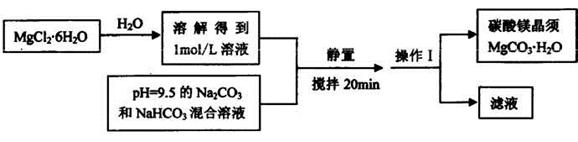
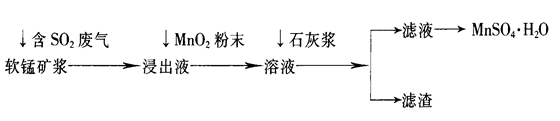
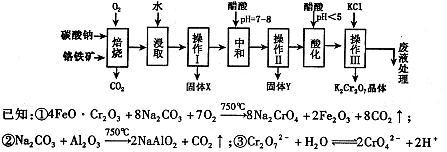

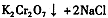 。该反应在溶液中能发生的理由是: 。
。该反应在溶液中能发生的理由是: 。