题目内容
16. 如图所示,各步反应的最后产物D是一种饱和一元醇,其蒸气密度是相同状况下H2密度的23倍,试回答下列问题:
如图所示,各步反应的最后产物D是一种饱和一元醇,其蒸气密度是相同状况下H2密度的23倍,试回答下列问题:(1)写出结构简式:ACH2═CH2,DCH3CH2OH.
(2)指出反应类型:⑥水解(取代)反应,⑧氧化反应.
(3)写出反应方程式:④CH3CH2OH
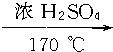 CH2═CH2↑+H2O,⑥CH3CH2Cl+H2O
CH2═CH2↑+H2O,⑥CH3CH2Cl+H2O CH3CH2OH+HCl,⑦CH3CHO+H2
CH3CH2OH+HCl,⑦CH3CHO+H2 CH3CH2OH,⑧2CH3CH2OH+O2
CH3CH2OH,⑧2CH3CH2OH+O2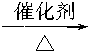 2CH3CHO+2H2O.
2CH3CHO+2H2O.
分析 D是一种饱和一元醇,其蒸气密度是相同状况下H2密度的23倍,即相对分子质量为46,所以D为CH3CH2OH,根据图中各物质转化关系及转化条件可知,A与水发生加成反应得乙醇,则A为CH2═CH2,乙烯与氯化氢发生加成反应生成B为CH3CH2Cl,CH3CH2Cl在碱性条件下发生水解(取代)反应得乙醇,乙烯氧化得C为CH3CHO,CH3CHO与氢气发生加成(还原)得乙醇,乙醇发生氧化反应得CH3CHO,据此答题.
解答 解:D是一种饱和一元醇,其蒸气密度是相同状况下H2密度的23倍,即相对分子质量为46,所以D为CH3CH2OH,根据图中各物质转化关系及转化条件可知,A与水发生加成反应得乙醇,则A为CH2═CH2,乙烯与氯化氢发生加成反应生成B为CH3CH2Cl,CH3CH2Cl在碱性条件下发生水解(取代)反应得乙醇,乙烯氧化得C为CH3CHO,CH3CHO与氢气发生加成(还原)得乙醇,乙醇发生氧化反应得CH3CHO,
(1)根据上面的分析可知,A为CH2═CH2,D为CH3CH2OH,
故答案为:CH2═CH2;CH3CH2OH;
(2)根据上面的分析可知,反应⑥为水解(取代)反应,反应⑧为氧化反应,
故答案为:水解(取代)反应;氧化反应;
(3)反应④的方程式为CH3CH2OH 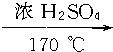 CH2═CH2↑+H2O,反应⑥的方程式为CH3CH2Cl+H2O
CH2═CH2↑+H2O,反应⑥的方程式为CH3CH2Cl+H2O
 CH3CH2OH,反应⑧的方程式为2CH3CH2OH+O2
CH3CH2OH,反应⑧的方程式为2CH3CH2OH+O2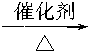 2CH3CHO+2H2O,
2CH3CHO+2H2O,
故答案为:CH3CH2OH 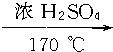 CH2═CH2↑+H2O;CH3CH2Cl+H2O
CH2═CH2↑+H2O;CH3CH2Cl+H2O
 CH3CH2OH;2CH3CH2OH+O2
CH3CH2OH;2CH3CH2OH+O2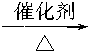 2CH3CHO+2H2O.
2CH3CHO+2H2O.
点评 本题考查有机物推断,注意根据D的性质进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.

 智能训练练测考系列答案
智能训练练测考系列答案| A. | NO+NO2+2NaOH=2NaNO2+H2O | B. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | ||
| C. | CuO+2HNO3═Cu(NO3)2+H2O | D. | 2FeCl2+Cl2=2FeCl3 |
| A. | 盐酸 | B. | 乙醇 | C. | 氢氧化钠 | D. | 硝酸 |
| A. | H2和Cl2 | B. | Cu和Cl2 | C. | H2和O2 | D. | Cu和O2 |
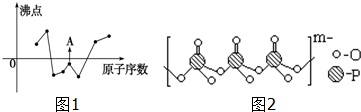
(2)如图1曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系.其中A点表示的单质是F2(填化学式).
| 键长/(pm) | B-F | B-Cl | B-Br |
| 计算值 | 152 | 187 | 199 |
| 实测值 | 130 | 175 | 187 |
(4)海产品添加剂多聚磷酸钠是由Na+与多聚磷酸根离子组成的,某种多聚磷酸根的结构如图2.
①磷原子的杂化类型为sp3.
②这种多聚磷酸钠的化学式为Nan+1PnO3n+1.
(5)已知HF与F-通过氢键结合成HF2-.判断HF2-和HF2-微粒间能否形成氢键,并说明理由.在HF2-中,已经存在分子内氢键(F-H…F-),所以没有可用于形成分子间氢键的氢原子,故HF2-和HF2-微粒间不能形成氢键.
| 选项 | 实验内容 | 实验目的 |
| A | 在食盐水中通入氟气置换出氯气 | 证明氟的非金属性强于氯 |
| B | 将滴有酚酞试液的氨水分成两份,并加热其中一份溶液 | 研究温度对弱电解质电离的影响 |
| C | 分别用玻璃棒蘸c(H+)相同的乙二酸和乙酸溶液,点在pH试纸上,并与标准比色卡对比 | 比较乙二酸和乙酸的酸性强弱 |
| D | 室温下,分别向体积、浓度均相同的Na2S2O3溶液中加入相同体积、不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 试管中加入少量苯,加入溴水振荡后,溴水褪色,发生了加成反应 | |
| B. | 苯能使酸性高锰酸钾溶液褪色 | |
| C. | 苯较难发生加成反应,所以通常要加入催化剂 | |
| D. | 苯不能发生取代反应 |
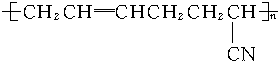 ,则这种高分子化合物的单体的结构简式是CH2=CHCH=CH2、CH2=CHCN.
,则这种高分子化合物的单体的结构简式是CH2=CHCH=CH2、CH2=CHCN.