题目内容
1.电解CuSO4和NaCl的混合溶液,开始阴极和阳极上分别析出的物质是( )| A. | H2和Cl2 | B. | Cu和Cl2 | C. | H2和O2 | D. | Cu和O2 |
分析 依据电解原理和溶液中的两种放电顺序分析判断;溶液中的阴离子向阳极移动,在阳极上放电;阳离子向阴极移动,在阴极上放电,并利用离子的放电顺序来分析阴极、阳极上分别析出的物质.
解答 解:用惰性电极电解NaCl与CuSO4的混合溶液,
溶液中Cl-、OH-、SO42-向阳极移动,Cl-放电能力最强,则2Cl--2e-═Cl2↑,
溶液中Cu2+、H+、Na+向阴极移动,Cu2+放电能力最强,则Cu2++2e-═Cu,
则在阴极、阳极上分别析出的物质为Cu与Cl2,
故选B.
点评 本题考查电解,注意利用惰性电极电解时溶液中离子的移动方向及离子的放电顺序是解答本题的关键,难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
11.将某合金(仅含铜、铁)全部投入50mL b mol•L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物),下列说法正确的是( )
| A. | 若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解 | |
| B. | 若金属全部溶解,则溶液中一定含有Fe3+ | |
| C. | 若硝酸有剩余,溶液中可能含有Fe2+ | |
| D. | 若金属全部溶解,且产生336mL气体(标准状况下),则b=0.3 |
10.去年下半年我省雾霾天气十分严重.PM2.5细颗粒物含有的毒性物质来源之一是汽车尾气排放.通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:NOx+CO$\stackrel{催化剂}{→}$N2+CO2,下列关于此反应的说法中,不正确的是( )
| A. | 所涉及元素的第一电离能:N>O>C | |
| B. | 当x=2时,每生成1molN2,转移电子数为4mol | |
| C. | 等物质的量N2和C02中,π键的个数比为1:1 | |
| D. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |

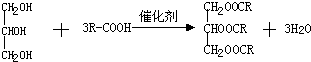 ;
;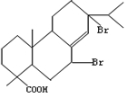 ;
;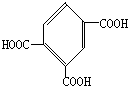 .
.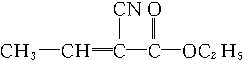 )涂在手术后的伤口上,数秒钟内可发生加聚反应而固化,是一种固化迅速的医用高分子缝合材料.这种化合物是由三种单体合成的.试回答:
)涂在手术后的伤口上,数秒钟内可发生加聚反应而固化,是一种固化迅速的医用高分子缝合材料.这种化合物是由三种单体合成的.试回答: .
.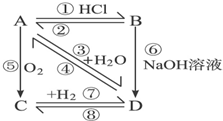 如图所示,各步反应的最后产物D是一种饱和一元醇,其蒸气密度是相同状况下H2密度的23倍,试回答下列问题:
如图所示,各步反应的最后产物D是一种饱和一元醇,其蒸气密度是相同状况下H2密度的23倍,试回答下列问题: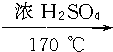 CH2═CH2↑+H2O,⑥CH3CH2Cl+H2O
CH2═CH2↑+H2O,⑥CH3CH2Cl+H2O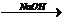 CH3CH2OH+HCl,⑦CH3CHO+H2
CH3CH2OH+HCl,⑦CH3CHO+H2 CH3CH2OH,⑧2CH3CH2OH+O2
CH3CH2OH,⑧2CH3CH2OH+O2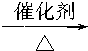 2CH3CHO+2H2O.
2CH3CHO+2H2O. 焰色反应是化学上用来测定某种金属是否存在于化合物的方法.
焰色反应是化学上用来测定某种金属是否存在于化合物的方法. ,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题: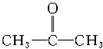 的官能团为
的官能团为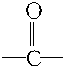 ,属于酮类物质,这两种物质的分子式为C3H6O,它们的关系是同分异构体.
,属于酮类物质,这两种物质的分子式为C3H6O,它们的关系是同分异构体.