题目内容
【题目】25℃时,取0.lmolL-1HA溶液与0.1molL-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因______(用离子方程式表示)。
(2)混合溶液中由水电离出的c(OH-)______0.1molL-1NaOH溶液中由水电离出的c(OH-)(填“>”、“<”或“=”)。
(3)所得混合液中各离子浓度从大到小的顺序为:______。
(4)混合液中:c(HA)+c(A-)=______molL-1。
(5)25℃时,已知NH4A溶液为中性,将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH______7(填“>”、“<”或“=”)。
(6)相同温度下相同物质的量浓度的下列四种盐溶液,pH由大到小的顺序______(填字母)。
A. NH4HCO3B. NH4AC. NH4HSO4D. NH4Cl
【答案】A-+H2OHA+OH- > c(Na+)>c(A-)>c(OH-)>c(H+) 0.05 > A>B>D>C
【解析】
0.lmol/LHA溶液与0.1mol/LNaOH溶液等体积混合,反应恰好生成NaA,混合溶液的pH=8,溶液为碱性,说明A-水解使溶液呈碱性,据此分析解答(1)~(4);
(5)NH4A溶液为中性,说明NH4+和A-的水解程度相当,将HA溶液加到Na2CO3溶液中有气体放出,说明酸性HA强于H2CO3,据此分析解答;
(6)NH4HSO4中电离出H+,酸性最强,NH4Cl为强酸弱碱盐,水解显酸性,NH4A为中性,酸性强弱HA>H2CO3,据此分析解答。
(1)0.lmol/LHA溶液与0.1mol/LNaOH溶液等体积混合,反应恰好生成NaA,混合溶液的pH=8,溶液为碱性,说明A-水解,A-+H2OHA+OH-,故答案为:A-+H2OHA+OH-;
(2)NaOH抑制水的电离,NaA水解促进水的电离,所以混合溶液中由水电离出的c(OH-)>0.1mol/LNaOH 溶液中由水电离出的c(OH-),故答案为:>;
(3)溶液呈碱性,则溶液中c(OH-)>c(H+),A-水解,所以溶液中离子浓度大小顺序为:c(Na+)>c(A-)>c(OH-)>c(H+),故答案为:c(Na+)>c(A-)>c(OH-)>c(H+);
(4)反应恰好生成NaA,混合液中存在物料守恒:c(HA)+c(A-)= c(Na+)=![]() =0.05mol/L,故答案为:0.05;
=0.05mol/L,故答案为:0.05;
(5)NH4A溶液为中性,说明NH4+和A-的水解程度相当,将HA溶液加到Na2CO3溶液中有气体放出,说明酸性HA强于H2CO3,则CO32-水解程度大于A-,因此CO32-水解程度大于NH4+,所以(NH4)2CO3溶液呈碱性,pH>7,故答案为:>;
(6)阴离子水解使溶液呈碱性,阳离子水解使溶液呈酸性,阳离子相同,比较阴离子水解程度,NH4HSO4中电离出H+,酸性最强,pH最小,酸性强弱HCl>HA>H2CO3,其中Cl-不水解,NH4Cl显酸性,水解程度A-<HCO3-,NH4A为中性,则NH4HCO3显碱性,因此pH由大到小的顺序为:A>B>D>C,故答案为:A>B>D>C。

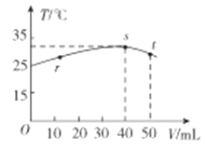
【题目】测定0.1 mol·L-1 Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。
下列说法不正确的是
A. Na2SO3溶液中存在水解平衡:![]() +H2O
+H2O![]()
![]() +OH
+OH
B. ④的pH与①不同,是由于![]() 浓度减小造成的
浓度减小造成的
C. ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D. ①与④的Kw值相等
【题目】测定![]() 溶液先升温再降温过程中的pH,数据如下。实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验。④产生白色沉淀多。下列说法不正确的是
溶液先升温再降温过程中的pH,数据如下。实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验。④产生白色沉淀多。下列说法不正确的是![]()
![]()
时刻 | ① | ② | ③ | ④ |
温度 | 25 | 30 | 40 | 25 |
pH |
|
|
| 9.25 |
A.![]() 溶液中存在水解平衡:
溶液中存在水解平衡:![]()
B.④的pH与①不同,是由于![]() 浓度减小造成的
浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D.①与④的![]() 值相等
值相等