题目内容
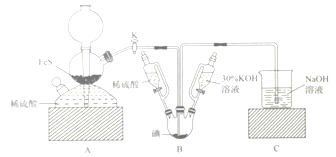
【题目】如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X(g)+Y(g)![]() 2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法正确的是( )
2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法正确的是( )

A. 反应开始时,B容器中化学反应速率快
B. A容器中X的转化率为40%,且比B容器中X的转化率小
C. 打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计)
D. 打开K达新平衡后,升高B容器温度,A容器体积一定增大
【答案】A
【解析】
A.起始VA=VB=aL,B中的物质的量大于A中的物质的量,即B装置中的浓度大于A装置中的浓度,所以反应开始时,B反应速率大于A反应速率,A正确;
B.等压、等温条件下,气体的体积之比大于气体的物质的量之比,达到平衡时,VA=1.2aL,所以平衡后混合气体的物质的量是2.4mol,设A物质反应了mmol。
X(g)+Y(g)![]() 2Z(g)+W(g)物质的量增多
2Z(g)+W(g)物质的量增多
1mol 1mol
mmol (2.4-2)mol=0.4mol
m=0.4,所以X物质的转化率=![]() =40%,而B装置是在等容条件下,反应向正反应方向移动时,使混合气体的物质的量增大,导致容器内气体压强增大,增大压强,平衡逆向移动,使物质X的转化率减小,所以A在物质X的转化率比B在X的转化率大,B错误;
=40%,而B装置是在等容条件下,反应向正反应方向移动时,使混合气体的物质的量增大,导致容器内气体压强增大,增大压强,平衡逆向移动,使物质X的转化率减小,所以A在物质X的转化率比B在X的转化率大,B错误;
C.当打开K时,整个装置是在等温、等压条件下反应,使整个装置中气体的压强与A装置中的初始压强相同时,A和B的体积之和为3aL,其中B占aL,则A占2aL;当等温等压条件下反应达到平衡状态时,混合气体的体积是原来的1.2倍,即混合气体的体积是3.6aL,其中B是aL,所以A是2.6aL,C错误;
D.不能确定该反应的正反应是放热反应还是吸热反应,所以升高温度,不能确定平衡移动方向,则A容器的容积可能增大,也可能减小,D错误;
故合理选项是B。

 口算题天天练系列答案
口算题天天练系列答案