题目内容
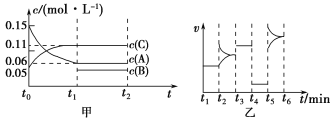
【题目】在盛有足量A的体积可变的密闭容器中通入B,发生反应:A(s)+ 2B(g)![]() 4C(g)+ D(g)△H>0,在一定温度、压强下达到平衡。平衡时C的物质的量与通入B的物质的量的变化关系如图所示。下列说法正确的是:( )
4C(g)+ D(g)△H>0,在一定温度、压强下达到平衡。平衡时C的物质的量与通入B的物质的量的变化关系如图所示。下列说法正确的是:( )
A.平衡时B的转化率为20%
B.若再通入B,则再次达平衡时C的体积分数增大
C.在容器中加入催化剂,则B的转化率增大
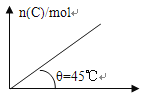
D.若保持压强一定,当温度升高时,图中θ>45°
【答案】D
【解析】
试题分析:根据在一定温度、压强下达到平衡,平衡时C的物质的量与加入B的物质的量的变化关系图可知,平衡时再加入B,因体积可变,则B的浓度不变,则平衡后B的加入平衡不移动;A为纯固体,则加入A不影响化学平衡的移动;该反应是吸热反应,升高温度平衡正向移动,则C的物质的量增加;再由图可知,达平衡时B、C的物质的量相等来计算B的转化率;A、设开始B的物质的量为n,转化的B为x,由图可知,达平衡时B、C的物质的量相等,则(n-x)=2x,n=3x,则B的转化率为x÷3x×100%=33.3%,A错误;B、因体积可变,则B的浓度不变,则v(正)、v(逆)都不变,B错误;C、因A为纯固体,加入A不影响化学平衡的移动,则B的转化率不变,C错误;D、压强一定,当升高温度时,平衡正向移动,则C的物质的量增加,由图可以看出,图中θ>45°,D正确;故选D.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目