题目内容
【题目】(1)通过火法冶金炼出的铜是粗铜,含杂质多,必须进行电解精炼。请在下面方框中画出电解精炼铜的装置______。

(2)水解反应在生产生活中有很多应用。有些盐水解程度很大,可以用于无机化合物的制备,如可以用TiCl4与H2O反应,生成TiO2·xH2O,制备时加入大量的水,同时加热。请结合化学用语和必要的文字解释“加热”的作用:______。
【答案】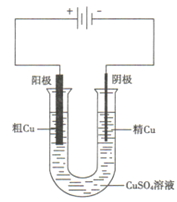 TiCl4+(x+2)H2O
TiCl4+(x+2)H2O![]() TiO2·xH2O↓+4HCl,水解是吸热的,加热使水解平衡右移,同时HCl挥发,促进水解反应趋于完全,制得TiO2·xH2O
TiO2·xH2O↓+4HCl,水解是吸热的,加热使水解平衡右移,同时HCl挥发,促进水解反应趋于完全,制得TiO2·xH2O
【解析】
(1)电解精炼铜时,粗铜作阳极,纯铜作阴极,电解质溶液是含有铜离子的盐溶液如硫酸铜溶液,因此电解装置为 ;
;
(2)TiCl4与H2O反应为TiCl4+(x+2)H2O![]() TiO2·xH2O↓+4HCl,加入大量水并加热,HCl挥发,促使水解正向进行,使水解反应趋于完全,从而制得TiO2xH2O。
TiO2·xH2O↓+4HCl,加入大量水并加热,HCl挥发,促使水解正向进行,使水解反应趋于完全,从而制得TiO2xH2O。

【题目】前四周期元素A、B、C、D、E的原子序数依次增大,基态A原子核外电子占据3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,C的双原子单质分子中σ键和π键数目之比为1:2,D的最高正化合价和最低负化合价之和等于4;基态E原子核外有6个未成对电子。
(1)基态E原子的核外电子排布式为______;基态D原子核外电子占据的能量最高的能级符号为_____________。
(2)A元素的各级电离能如下:
能级(I) | I1 | I2 | I3 | I4 | I5 |
电离能/kJ·mol-1 | 800.6 | 2427 | 3660 | 25026 | 32827 |
分析上表数据知,相邻两个电子的电离能中,I3和I4之间差异最大,其主要原因是__________。
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是________。
(4)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp3杂化、立体构型为三角锥形的是_______(填分子式)。
(5)(DC)4为热色性固体,且有色温效应。低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是____;在常压下,(DC)4高于130℃分解为相应的单质,这一变化中破坏的作用力是_______。在B、C、D的简单气态氢化物中,属于非极性分子的是______(填分子式,下同),常与Cu2+、Zn2+、Ag+等形成配离子的是_______________。
(6)A、C形成立方晶体,晶体结构类似金刚石,如图所示。已知:该晶体密度为ρg·㎝-3,NA代表阿伏伽德罗常数的值。

①该晶体的化学式为__________。
②在该晶体中,A与C形成共价键的键长(d)为_____pm。