题目内容
短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素.试回答下列问题:
(1)A在元素周期表中的位置是
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是
(3)CA2与D元素的单质在水溶液中反应的离子方程式是:
(4)C元素常见的化合价有-2、+2、+4、+6等,C与A、B、D均能两两形成各原子(或离子)都满足最外层8电子稳定结构的化合物.请你大胆猜想,写出其中两种化合物的化学式
(1)A在元素周期表中的位置是
第二周期ⅥA族
第二周期ⅥA族
.(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是
S2->O2->Na+
S2->O2->Na+
(填离子符号) (3)CA2与D元素的单质在水溶液中反应的离子方程式是:
SO2+Cl2+2H2O=4H++2Cl-+SO42-
SO2+Cl2+2H2O=4H++2Cl-+SO42-
.(4)C元素常见的化合价有-2、+2、+4、+6等,C与A、B、D均能两两形成各原子(或离子)都满足最外层8电子稳定结构的化合物.请你大胆猜想,写出其中两种化合物的化学式
Na2S
Na2S
、Na2S2
Na2S2
.分析:A原子的最外层电子数是次外层电子数的3倍,则原子核各层电子分别为2、6,应为O元素,A、C同主族,则C为S元素,B、C、D同周期,且B是短周期元素中原子半径最大的主族元素,则B为Na元素,D为Cl元素,根据原子结构以及对应的单质化合物的性质结合元素周期律的递变规律可解答该题.
解答:解:A原子的最外层电子数是次外层电子数的3倍,则原子核各层电子分别为2、6,应为O元素,A、C同主族,则C为S元素,B、C、D同周期,且B是短周期元素中原子半径最大的主族元素,则B为Na元素,D为Cl元素,则
(1)A为O元素,原子核外有2个电子层,最外层电子数为6,则位于周期表第二周期ⅥA族,
故答案为:第二周期ⅥA族;
(2)A、B、C三种元素形成的简单离子分别为O2-、Na+、S2-,其中S2-比O2-多一个电子层,则半径:S2->O2-,O2-和Na+核外电子排布相同,根据核电核数越大,半径越小可知半径O2->Na+,所以:S2->O2->Na+,
故答案为:S2->O2->Na+;
(3)SO2具有还原性,Cl2具有氧化性,二者在溶液中发生氧化还原反应生成HCl和H2SO4,反应的离子方程式为SO2+Cl2+2H2O=4H++2Cl-+SO42-,
故答案为:SO2+Cl2+2H2O=4H++2Cl-+SO42-;
(4)C为S元素,B为Na元素,D为Cl元素,其中形成的化合物最外层满足最外层8电子稳定结构的有Na2S、Na2S2、SCl2、S2Cl2等,
故答案为:Na2S、Na2S2、SCl2、S2Cl2等(任意二者).
(1)A为O元素,原子核外有2个电子层,最外层电子数为6,则位于周期表第二周期ⅥA族,
故答案为:第二周期ⅥA族;
(2)A、B、C三种元素形成的简单离子分别为O2-、Na+、S2-,其中S2-比O2-多一个电子层,则半径:S2->O2-,O2-和Na+核外电子排布相同,根据核电核数越大,半径越小可知半径O2->Na+,所以:S2->O2->Na+,
故答案为:S2->O2->Na+;
(3)SO2具有还原性,Cl2具有氧化性,二者在溶液中发生氧化还原反应生成HCl和H2SO4,反应的离子方程式为SO2+Cl2+2H2O=4H++2Cl-+SO42-,
故答案为:SO2+Cl2+2H2O=4H++2Cl-+SO42-;
(4)C为S元素,B为Na元素,D为Cl元素,其中形成的化合物最外层满足最外层8电子稳定结构的有Na2S、Na2S2、SCl2、S2Cl2等,
故答案为:Na2S、Na2S2、SCl2、S2Cl2等(任意二者).
点评:本题考查元素的推断以及元素化合物知识,解答本题时注意把握原子的结构特点,结合元素周期律知识进行推断,题目难度中等,易错点为(4).

练习册系列答案
相关题目
短周期主族元素A、B、C、D的原子序数依次增大.A、C原子序数相差8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A、原子半径:A<D<C<B | B、B、C、D分别与A形成的化合物一定含有相同的化学键 | C、最高价氧化物对应水化物的酸性:D<C | D、常温下,单质B能大量溶于浓硝酸中 |
短周期主族元素A、B、C的原子序数依次递增,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,它们原子的最外层电子数之和为10,则下列叙述正确的是( )
| A、原于半径A<B<C | B、A的气态氢化物稳定性大于C的气态氢化物稳定性 | C、A、C两元素最高价氧化物均可与水化合得到对应的酸 | D、高温时,A单质可以从C的氧化物中置换得到C单质 |
短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质为淡黄色固体.下列推断中正确的是( )
| A、原子半径由小到大的顺序:r(C)<r(D)<r(E) | B、元素D、E分别与A形成的化合物的热稳定性:E>D | C、元素D的最高价氧化物对应水化物的酸性比E的强 | D、元素B分别与A、C形成的化合物中化学键的类型完全相同 |
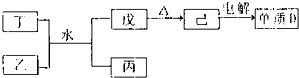
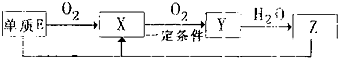
 短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物.
短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物. NH3?H2O+H+
NH3?H2O+H+ 2NO2
2NO2