题目内容
设NA为阿伏加德罗常数的值,下列叙述不正确的( )
| A.5g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA |
| B.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C.50 mL 12 mol?L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| D.常温常压下,46g NO2 与N2O4的混合气体中含有的原子总数为3NA |
C
解析试题分析:A、5g质量分数为46%的乙醇溶液中,乙醇的质量=5g×46%=2.3g,物质的量=2.3g÷46g/mol=0.05mol,氢原子的物质的量=0.05mol×6=0.3mol。水的质量=5g-2.3g=2.7g,水的物质的量=2.7g÷18g/mol=0.15mol,氢原子的物质的量=0.15mol×2=0.3mol,所以氢原子总的物质的量是0.6mol,则氢原子的总数为0.6NA,A正确;B、5.6g铁的物质的量是0.1mol,与0.1mol氯气反应时铁过量,氯气完全反应,所以反应中转移电子数为0.2NA,C不正确;D、NO2与N2O4的最简式相同,均是NO2,所以46g NO2 与N2O4的混合气体中含有的原子的物质的量=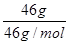 ×3=3mol,其原子总数为3NA,D正确,答案选C。
×3=3mol,其原子总数为3NA,D正确,答案选C。
考点:考查阿伏加德罗常数的有关计算。

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.11.2 L氧气中所含有的原子数为NA |
| B.同温同压下,NA个NO2与NA个N2和O2的混合气体的体积不相等 |
| C.物质的量浓度为0.5 mol·L-1的MgCl2溶液中,含有Cl-个数为NA |
| D.54 g Al分别与足量的稀硫酸及氢氧化钠溶液反应失去的电子数都是6NA |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.25℃时,pH=13的氨水中含有OH-的数目为0.1NA |
| B.标准状况下,2.24 LNO2与水反应生成NO3-的数目为0.1NA |
| C.1 mol Na被完全氧化生成Na2O2,转移电子的数目为NA |
| D.4.0 g H2与足量O2完全反应生成水,反应中断裂共价键的总数为2NA |
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
| A.若M(甲)>M(乙),则气体体积:甲<乙 |
| B.若M(甲)<M(乙),则气体的压强:甲>乙 |
| C.若M(甲)>M(乙),则气体的摩尔体积:甲<乙 |
| D.若M(甲)<M(乙),则的分子数:甲<乙 |
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3,溶质的质量分数为ω,溶质的物质的量浓度为c mol/L。下列叙述中正确的是( )
| A.ω=35a/(22.4Vρ) |
| B.c =a/(22.4V)mol/L |
| C.上述氨水中再加入等体积等浓度的稀盐酸后溶液恰好呈中性 |
| D.上述氨水中再加入V mL水后,所得溶液的质量分数小于0.5ω |
设NA为阿佛加德罗常数的数值,下列说法正确的是
| A.常温常压下,8gO2含有4NA个电子 |
| B.1L1mol·L-1的NaClO 溶液中含有ClO-的数目为NA |
| C.标准状况下,22.4L盐酸含有NA个HCl分子 |
| D.1molNa被完全氧化生成Na2O2,失去2NA个电子 |
设NA为阿佛加德罗常数的值,下列叙述正确的是
| A.常温下 ,4gCH4含有NA 个C-H共价键 |
| B.1 mol Fe 与足量的稀HNO3反应,转移2 NA个电子 |
| C.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| D.某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
下列溶液中Cl-浓度最大的是( )
| A.10ml 0.2mol/L的FeCl3溶液 |
| B.10ml 0.1mol/L的AlCl3溶液 |
| C.20ml 0.1mol/L的MgCl2溶液 |
| D.20ml 0.1mol/L的HCl溶液 |
用NA表示阿伏德罗常数,下列叙述正确的是
| A.标准状况下,22.4LH2O含有的分子数为1 NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C.通常状况下,1 NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol·/L的MgCl2溶液中,含有Cl-个数为1 NA |