题目内容
将含有0.1 mol SiO2的铝、硅混合物分别与足量NaOH溶液、盐酸混合,充分反应后前者可得到11.2 L气体(标准状况),后者可得到6.72 L气体(标准状况),则参加反应的n(HCl)与n(NaOH)之比为( )。
| A.1∶1 | B.1∶2 | C.2∶1 | D.3∶1 |
A
混合物与足量NaOH溶液反应生成的n(H2)1=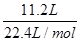 =0.5 mol,混合物与足量盐酸反应生成的n(H2)2=
=0.5 mol,混合物与足量盐酸反应生成的n(H2)2=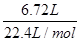 =0.3 mol,混合物中只有铝能与盐酸反应,由此可求出n(Al)=
=0.3 mol,混合物中只有铝能与盐酸反应,由此可求出n(Al)= n(H2)=0.2 mol,硅、铝均能与NaOH溶液反应且铝与NaOH溶液反应放出的氢气也是0.3 mol,故硅与NaOH溶液反应放出的氢气是0.2 mol,由此可求出n(Si)=0.1 mol。铝完全反应消耗0.6 mol HCl,三种物质与NaOH溶液反应,消耗0.6 mol NaOH,故n(HCl)∶n(NaOH)=1∶1。
n(H2)=0.2 mol,硅、铝均能与NaOH溶液反应且铝与NaOH溶液反应放出的氢气也是0.3 mol,故硅与NaOH溶液反应放出的氢气是0.2 mol,由此可求出n(Si)=0.1 mol。铝完全反应消耗0.6 mol HCl,三种物质与NaOH溶液反应,消耗0.6 mol NaOH,故n(HCl)∶n(NaOH)=1∶1。
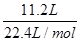 =0.5 mol,混合物与足量盐酸反应生成的n(H2)2=
=0.5 mol,混合物与足量盐酸反应生成的n(H2)2=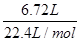 =0.3 mol,混合物中只有铝能与盐酸反应,由此可求出n(Al)=
=0.3 mol,混合物中只有铝能与盐酸反应,由此可求出n(Al)= n(H2)=0.2 mol,硅、铝均能与NaOH溶液反应且铝与NaOH溶液反应放出的氢气也是0.3 mol,故硅与NaOH溶液反应放出的氢气是0.2 mol,由此可求出n(Si)=0.1 mol。铝完全反应消耗0.6 mol HCl,三种物质与NaOH溶液反应,消耗0.6 mol NaOH,故n(HCl)∶n(NaOH)=1∶1。
n(H2)=0.2 mol,硅、铝均能与NaOH溶液反应且铝与NaOH溶液反应放出的氢气也是0.3 mol,故硅与NaOH溶液反应放出的氢气是0.2 mol,由此可求出n(Si)=0.1 mol。铝完全反应消耗0.6 mol HCl,三种物质与NaOH溶液反应,消耗0.6 mol NaOH,故n(HCl)∶n(NaOH)=1∶1。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
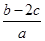 mol·L-1
mol·L-1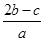 mol·L-1
mol·L-1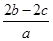 mol·L-1
mol·L-1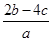 mol·L-1
mol·L-1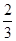 NA个NO分子
NA个NO分子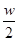 g水,得到4a% NaCl溶液
g水,得到4a% NaCl溶液