题目内容
【题目】一种驱动潜艇的液氨-液氧燃料电池原理示意如图,下列有关该电池说法正确的是( )
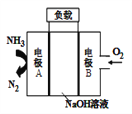
A. 电流由电极A经外电路流向电极B
B. 电池工作时,OH-向电极B移动
C. 该电池工作时,每消耗22.4L NH3转移3mol电子
D. 电极A上发生的电极反应为:2NH3-6e-+ 6OH-=N2 + 6H2O
【答案】D
【解析】A、由图可知,NH3被氧化为N2,发生氧化反应,所以该电池中A是负极,B是正极,电流由正极(B)流向负极(A),故A错误;B、原电池中,阴离子向负极移动,则OH﹣向负极A移动,故B错误;C、气体的体积必须标明温度和压强,否则没有意义,故C错误;D、碱性条件下,A电极发生NH3转化为N2,故电极反应为: 4NH3+3O2=2N2+6H2O,故D正确。故选D。

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案【题目】下列关于氯水的叙述,不正确的是( )
A. 新制的氯水中,溶质既有分子又有离子
B. 新制的氯水是无色透明的液体,有酸性和漂白性
C. 光照氯水有气泡逸出,该气体是O2
D. 氯水放置数天后酸性将增强
【题目】汽车尾气中通常含有NxOy和CO等大气污染物,科学家寻找高效催化剂实现了汽车尾气的转化进而减少汽车尾气对大气的污染。
(1)己知:①CO的燃烧热△H1=-283kJ·mol-1 ②N2(g)+O2(g) =2NO(g) △H2 =+183kJ·mol-1
由此写出NO和CO反应的热化学反应方程式________________________________。
(2)一定温度下,向2L密闭容器中充入4.0mo1NO2和4.0molCO,在催化剂作用下发生反应 4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) △H<0,测得相关数据如下:
N2(g)+4CO2(g) △H<0,测得相关数据如下:
0 min | 5 min | 10 min | 15 min | 20 min | |
c(NO2)/ mol·L-1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
C(N2)/ mol·L-1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①5l0min,用N2的浓度变化表示的反应速率为__________________。
②以下表述能说明该反应己达到平衡状态的是________。
A.气体颜色不再变化 B.气体密度不再变化 C.气体平均相对分子质量不再变化
③20 min时,保持温度不变,继续向容器中加入1.0mol NO2和1.0molCO,在t1时刻反应再次达到平衡,则NO2的转化率比原平衡 ______________(填“增大”、“减小”或“不变)。
④该温度下反应的化学平衡常数K= __________ (保留两位有效数字)。
(3)CO、空气与过量KOH溶液可构成燃料电池(石墨为电极):
①写出该电池的负极反应式____________________________;
②常温下,用该燃料电池电解(惰性电极)1L饱和食盐水(足量),当两极共生成4.48L (折算为标准状况)气体时电解池溶液的pH=__________。(忽略溶液的体积变化,己知1g2=0.3,lg5=0.7)