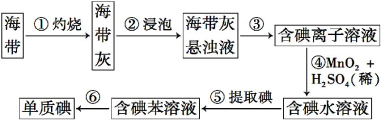
题目内容
【题目】某同学在研究Fe与H2SO4的反应时,进行了如下实验。
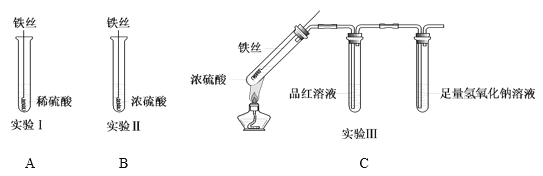
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为______。
(2)实验Ⅱ中,铁丝表面迅速变黑,反应很快停止,其原因是______。
(3)实验Ⅲ中,加热后产生大量气体,A试管中溶液的红色褪去,C处始终未检测到可燃性气体。B试管中反应的离子方程式是______。
(4)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同。浓硫酸的氧化性源于+6价的硫元素,稀硫酸的氧化性源于______。
②造成反应多样性的主要因素有______。
【答案】Fe+2H+=== Fe2++H2↑ 铁表面生成致密的氧化膜,阻止反应进一步进行 SO2+2OH—=== SO3+H2O +1价的氢元素 反应物的浓度、温度
【解析】
(1)Fe和稀硫酸反应生成硫酸亚铁和氢气;
(2)浓硫酸具有强氧化性,发生钝化;
(3)铁与稀硫酸反应生成氢气,和浓硫酸共热反应生成二氧化硫,二氧化硫使品红溶液的红色褪去,二氧化硫与氢氧化钠溶液反应生成亚硫酸钠,未检测到可燃性气体,说明反应中没有氢气生成;
(4)①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性表现在+6价的硫元素上,稀硫酸的氧化性表现在+1价的氢元素上;
②影响反应产物多样性的因素有浓度、温度、反应物的量等。
(1)Fe和稀硫酸反应生成硫酸亚铁和氢气,离子方程式为Fe+2H+=Fe2++H2↑,
故答案为:Fe+2H+=Fe2++H2↑;
(2)浓硫酸具有强氧化性,生成致密的氧化膜覆盖在Fe的表面,发生钝化,
故答案为:钝化;
(3)实验Ⅲ中,铁与稀硫酸反应生成氢气,和浓硫酸共热反应生成二氧化硫,实验中未检测到可燃性气体,说明反应中没有氢气生成,二氧化硫具有漂白性,使品红溶液的红色褪去,二氧化硫是酸性氧化物,与氢氧化钠溶液反应生成亚硫酸钠,反应的离子方程式为SO2+2OH—=SO32—+H2O,故答案为:SO2+2OH—=SO32—+H2O;
(4)①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性表现在+6价的硫元素上,稀硫酸的氧化性表现在+1价的氢(H+)元素上,故答案为:+6价S元素,+1价H元素(H+);
②影响反应产物多样性的因素有浓度、温度、反应物的量等,故答案为:浓度、温度、反应物的量等。

【题目】某学生用已知物质的量浓度的标准盐酸测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制500mL溶液。除烧杯、量筒、胶头滴管和玻璃棒外,还需要的玻璃仪器是___________。取用25.00mL待测液时需要的仪器是_____________。
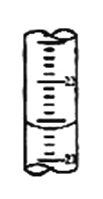
(2)滴定过程中,在锥形瓶底垫一张白纸的作用是_______________;若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50mL,滴定后液面如图(上面数字:22,下面数字:23)。,则此时消耗标准溶液的体积为_________mL
(3)下列操作中可能使所测NaOH溶液的浓度数值偏高的是________。
A.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净但没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
(4)用标准盐酸滴定上述待测NaOH溶液时,判定滴定终点的现象是:直到加入最后一滴盐酸,_____________________________为止。
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.28 | 26.28 |
第二次 | 25.00 | 1.55 | 31.30 | 29.75 |
第三次 | 25.00 | 0.20 | 26.42 | 26.22 |
计算该NaOH溶液的物质的量浓度:c(NaOH)=__________mol/L。(保留四位有效数字)