题目内容
1.一个价电子构型为2s22p5的元素,下列有关其描述正确的有( )| A. | 位于第2周期ⅦA族 | B. | 原子序数为7 | C. | 有最高正价+7 | D. | 电负性最大 |
分析 价电子构型为2s22p5的元素为F元素,F元素位于第2周期ⅦA族,原子序数为9,没有最高正化合价,是电负性最强的元素.
解答 解:价电子构型为2s22p5的元素为F元素.
A.F元素位于第2周期ⅦA族,故A正确;
B.原子序数为9,故B错误;
C.F元素没有最高正价+7,故C错误;
D.F的非金属性最强,电负性最强,故D正确;
故选:AD.
点评 本题考查原子结构与元素周期律,侧重于原子结构与元素周期律的递变规律的考查,难度不大,注意把握元素周期律知识.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.自来水可用氯气消毒,用这种自来水配制下列物质溶液,不会产生明显的药品变质问题的是( )
| A. | AgNO3溶液 | B. | NaCl | C. | FeCl2 | D. | NaOH |
9.下列有关叙述正确的是( )
| A. | H、D、T具有相同的质子数,是氢元素的三种同位素 | |
| B. | OH-与H3O+组成元素相同,所含质子数相同 | |
| C. | 结构示意图为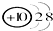 和 和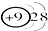 两种粒子为同一种元素 两种粒子为同一种元素 | |
| D. | 元素原子最外层电子数的多少是判断金属性和非金属性强弱的依据 |
16.用铁片和稀硫酸反应时,下列措施不能使生成氢气的速率加快的是( )
| A. | 对该反应体系加热 | B. | 不用稀硫酸,改用98%的浓硫酸 | ||
| C. | 加少量CuSO4溶液 | D. | 不用铁片,改用铁粉 |
6.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 4.6gNO2和N2O4的混合气体中氧原子数小于0.2NA | |
| B. | 1 L 0.1 mol.L-1的Na2S溶液中离子总数小于0.3NA | |
| C. | 在标况下,2.24 L CCl4含有0.4NA个Cl原子 | |
| D. | 0.1 mol H2O2参加氧化还原反应时,不一定转移0.2NA个电子 |
4.下列有机物命名正确的是( )
| A. |  2-乙基丙烷 2-乙基丙烷 | B. | 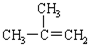 2-甲基-2-丙烯 2-甲基-2-丙烯 | ||
| C. | 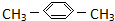 间二甲苯 间二甲苯 | D. | CH3CH2CH2CH2OH 1-丁醇 |
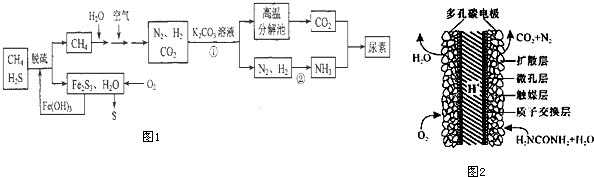
5. 质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种.如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是( )
质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种.如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是( )
 质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种.如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是( )
质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种.如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是( )| A. | 溶液中H+透过质子交换膜从右向左迁移 | |
| B. | 正极反应式为:O2+2H2O+4e-=4OH- | |
| C. | 电子从a极流出经电解质溶液流到b极 | |
| D. | 该电池在使用过程中,H+的物质的量保持不变 |