题目内容
【题目】某同学进行实验研究时,需要配制500mL 0.1molL﹣1 Na2CO3溶液.
(1)经过计算,使用托盘天平应该称量______g Na2CO3固体;
(2)配制溶液时,除了托盘天平、药匙、量筒、烧杯、玻璃棒外,还需要的仪器有______;
(3)配制溶液时,需经过称量、溶解、转移溶液、______、定容、摇匀等操作.下列图示对应的操作规范的一个是______;
A 称量
B 溶解
C 转移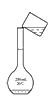
D 转移![]()
(4)误差(填偏高、偏低、无影响)
若配制溶液时,洗干净的容量瓶中残留有少量蒸馏水,则所配溶液的浓度______;若摇匀后发现液面低于刻度线,又加入少量蒸馏水与刻度线相平,则所配溶液的浓度______.
【答案】5.3 500mL容量瓶、胶头滴管 洗涤 B 无影响 偏低
【解析】
(1)依据m=CVM计算需要溶质的质量;
(2)配制500mL 0.1molL﹣1 Na2CO3溶液,需要选用500mL容量瓶,根据配制溶液的一般步骤判断使用的仪器;
(3)依据配制一定物质的量浓度溶液的一般步骤解答;
A.称量固体应遵循左物右码;
B.溶解时,应用玻璃棒搅拌加速溶解,注意玻璃棒沿着一个方向搅拌;
C.移液应用玻璃棒引流;
D.定容时,胶头滴管不能插入容量瓶内部;
(4)分析操作对溶质的物质的量和溶液的体积的影响,依据C=![]() 进行误差分析。
进行误差分析。
(1)配制500mL 0.1molL﹣1 Na2CO3溶液,应称取碳酸钠的质量m=0.1mol/L×0.5L×106g/mol=5.3g;
(2)配制的为500mL 0.10mol/LNa2CO3溶液,配制步骤为:计算→称量→溶解→转移→洗涤→定容→摇匀→保存到试剂瓶中,使用的仪器有:托盘天平、烧杯、玻璃棒、量筒、药匙、500mL容量瓶、胶头滴管,还需要的仪器有:500mL容量瓶、胶头滴管;
(3)配制溶液的一般步骤:计算→称量→溶解→转移→洗涤→定容→摇匀→保存到试剂瓶中;
A.称量固体应遵循左物右码;
B.溶解时,应用玻璃棒搅拌加速溶解,注意玻璃棒沿着一个方向搅拌;
C.移液应用玻璃棒引流;
D.定容时,胶头滴管不能插入容量瓶内部;
故答案为:B;
(4)若配制溶液时,洗干净的容量瓶中残留有少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变;若摇匀后发现液面低于刻度线,又加入少量蒸馏水与刻度线相平,导致溶液体积偏大,溶液浓度偏低。

【题目】如图,利用培养皿探究SO2的性质。实验时向Na2SO3固体上滴几滴浓硫酸,立即用另一表面皿扣在上面。
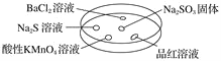
下表中对实验现象的描述或所做的解释不正确的是( )
选项 | 实验现象 | 解释 |
A | BaCl2溶液变浑浊 | SO2与BaCl2溶液反应产生了BaSO3沉淀 |
B | Na2S溶液变浑浊 | SO2与Na2S溶液反应产生了S单质 |
C | 酸性KMnO4溶液褪色 | SO2具有还原性 |
D | 品红溶液褪色 | SO2具有漂白性 |
A. A B. B C. C D. D
【题目】干燥剂的干燥性能可用干燥干燥效率(1立方米空气中实际余留水蒸气的质量![]() 来衡量
来衡量![]() 某些干燥剂的干燥效率如下:
某些干燥剂的干燥效率如下:
物质 | MgO | CaO | ZnCl2 | ZnBr2 |
干燥效率 | 0.008 | 0.2 | 0.8 | 1.1 |
根据以上数据,有关叙述错误的是
A. MgO的干燥性能比CaO差 B. 干燥效率可能与干燥剂的阴阳离子半径大小有关
C. MgCl2可能是比CaCl2更好的干燥剂 D. 上述干燥剂中阳离子对干燥性能的影响比阴离子大