题目内容
在一定温度下将100mLN2,H2混合气充入密闭恒压容器内,发生反应达到平衡时维持温度不变,测得混合气的密度是反应前密度的1.25倍,平均分子量为15.5。求平衡时N2的转化率;N2,H2两种气体开始时各为多少毫升?
平衡时N2的转化率25%;N2,H2两种气体开始的体积分别为40mL和60mL。
∵同T同P下有(ρ1/ρ2)=(m1/m2)
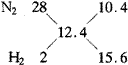
∴有(1/1.25)=(m1/15.5)?解得m1=12.4
(V1/V2)=(n1/n2)
即:?VN2∶VH2=10.4∶15.6
∴?VN2=10.4/(10.4+15.6)×100mL=40mL
??VH2=100mL-40mL=60mL
设N2转化的体积为x,则有:
?????N2? + ?3H2 2NH3
2NH3
起始体积 40 60 0
转化体积 x 3x 2x
平衡体积 40-x 60-3x 2x
?V总=40-x+60-3x+2x=100-2x
∴有:
15.5=((40-x)×28+(60-3x)×2+2x×17)/(100-2x)
解得?x=10mL
∴N2的转化率为:
N2%=(10/40)×100%=25%

∴有(1/1.25)=(m1/15.5)?解得m1=12.4
(V1/V2)=(n1/n2)
即:?VN2∶VH2=10.4∶15.6
∴?VN2=10.4/(10.4+15.6)×100mL=40mL
??VH2=100mL-40mL=60mL
设N2转化的体积为x,则有:
?????N2? + ?3H2
 2NH3
2NH3起始体积 40 60 0
转化体积 x 3x 2x
平衡体积 40-x 60-3x 2x
?V总=40-x+60-3x+2x=100-2x
∴有:
15.5=((40-x)×28+(60-3x)×2+2x×17)/(100-2x)
解得?x=10mL
∴N2的转化率为:
N2%=(10/40)×100%=25%

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
 2Z(g)(正反应为吸热反应)。已知X的转化率为20%时温度为100 ℃。如果温度提高一倍时转化率也增大一倍,平衡时当反应物总物质的量和生成物总物质的量相等时温度应为多少?
2Z(g)(正反应为吸热反应)。已知X的转化率为20%时温度为100 ℃。如果温度提高一倍时转化率也增大一倍,平衡时当反应物总物质的量和生成物总物质的量相等时温度应为多少?
 2C + D + Q,此时,A,B,C的物质的量均为amol,而D的物质的量为dmol。改变a的取值,再通过改变反应的条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2与2d之间变化,则a的取值范围应是__________________________(用a和d的关系式表示)。
2C + D + Q,此时,A,B,C的物质的量均为amol,而D的物质的量为dmol。改变a的取值,再通过改变反应的条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2与2d之间变化,则a的取值范围应是__________________________(用a和d的关系式表示)。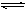 2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。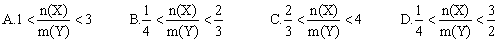
 CO(g)+H2O(g)(正反应吸热),反应达到平衡后,由于条件的改变而引起正、逆反应速率的变化,以及平衡移动的状况,据图可知,改变的条件是( )
CO(g)+H2O(g)(正反应吸热),反应达到平衡后,由于条件的改变而引起正、逆反应速率的变化,以及平衡移动的状况,据图可知,改变的条件是( )