题目内容
某温度下N2O4和NO2之间建立起如下的平衡N2O4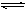 2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
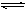 2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。N2O4的分解率为20%。
设N2O4的起始物质的量为1
转化了的N2O4物质的量为x
???????N2O4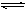 2NO2
2NO2
起始物质的量??1?????0
转化物质的量??x????2x
平衡物质的量??1-x???2x
平衡时混合气体的总物质的量为
n总=1-x+2x=1+x
∵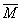 =29·D=29×2.644=76.68
=29·D=29×2.644=76.68
已知N2O4和NO2的相对分子质量分别为92,46,则有:
76.68=(92×(1-x)+46×2x/1+x)
解得x=0.2mol
∴N2O4的分解率为:(0.2/1)×100%=20%
转化了的N2O4物质的量为x
???????N2O4
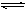 2NO2
2NO2起始物质的量??1?????0
转化物质的量??x????2x
平衡物质的量??1-x???2x
平衡时混合气体的总物质的量为
n总=1-x+2x=1+x
∵
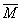 =29·D=29×2.644=76.68
=29·D=29×2.644=76.68已知N2O4和NO2的相对分子质量分别为92,46,则有:
76.68=(92×(1-x)+46×2x/1+x)
解得x=0.2mol
∴N2O4的分解率为:(0.2/1)×100%=20%

练习册系列答案
相关题目
 2SO3;ΔH<0,此时活塞已保持静止,SO2反应速率为v0。再往A内迅速充入2 mol SO2和1 mol O2,当活塞再次保持静止时,SO2反应速率为v,在此过程中,下列说法正确的是
2SO3;ΔH<0,此时活塞已保持静止,SO2反应速率为v0。再往A内迅速充入2 mol SO2和1 mol O2,当活塞再次保持静止时,SO2反应速率为v,在此过程中,下列说法正确的是
 2C达到平衡时,增大压强,C的量减少,则下列结论符合该平衡的是( )
2C达到平衡时,增大压强,C的量减少,则下列结论符合该平衡的是( ) 2SCl2(鲜红色液体);△H=+61.16kJ。
2SCl2(鲜红色液体);△H=+61.16kJ。 2NH3。下列有关说法正确的是( )
2NH3。下列有关说法正确的是( )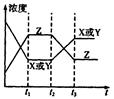
 2C(g)(正反应为放热反应),在一定温度下,反应物B的转化率与压强有如图所示的关系,那么n值一定是…( )
2C(g)(正反应为放热反应),在一定温度下,反应物B的转化率与压强有如图所示的关系,那么n值一定是…( )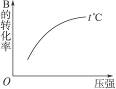
 2H2O与2H2O
2H2O与2H2O 2H2↑+O2↑
2H2↑+O2↑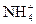 +OH-
+OH-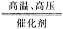 3H2+N2与N2+3H2
3H2+N2与N2+3H2 2NH3
2NH3 2SO3与2SO3
2SO3与2SO3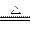 H2↑+I2↑与H2+I2
H2↑+I2↑与H2+I2