题目内容
【题目】关于下列图象及其相关说法正确的是( )
图①: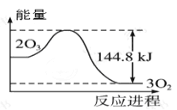 图②:
图②: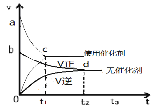
图③: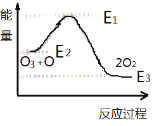 图④ :
图④ :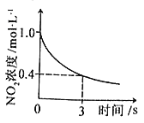
A.据图①可判断:2O3(g)=3O2(g);△H= - 44.8KJ/mol
B.据图②可判断:某反应在使用催化剂时比无催化剂时反应速率大,且面积Saco>Sbdo
C.据图③可判断: 2O2(g)═O3(g)+O(g)△H>0
D.据图④可判断:2NO2(g)+O3(g) ![]() N2O5(g)+O2(g),0~3s内,反应速率为V(N2O5)=0.2mol·L-1·S-1
N2O5(g)+O2(g),0~3s内,反应速率为V(N2O5)=0.2mol·L-1·S-1
【答案】C
【解析】
试题分析:A、焓变等于生成物的总能量减去反应物的总能量,则根据图无法判断:2O3(g)=3O2(g)的焓变,故A错误;B、催化剂只改变反应速率,不改变平衡移动,所以面积Saco=Sbdo,故B错误;C.反应物的总能量高于生成物的总能量,反应放热,故△H<0,其逆反应的△H>0,故C正确;D.由图可知,0-3s内,二氧化氮的浓度变化量=1mol/L-0.4mol/L=0.6mol/L,故v(NO2)=![]() =0.2mol/(L.s),V(N2O5)=
=0.2mol/(L.s),V(N2O5)=![]() v(NO2)=0.1mol/(L.s),故D错误,故选C。
v(NO2)=0.1mol/(L.s),故D错误,故选C。

【题目】《石雅》云:“青金石色相如天,或复金屑散乱,光辉灿烂,若众星丽于天也。”天为上,所以中国古代通常称青金石为帝王石,明淸尤重。青金石是指碱性铝硅酸盐矿物,其中含钠、铝、硅、硫、氯、氧等元素。
(1)铝元素基态原子的外围电子轨道表示式为_____________,基态硅原子核外电子占有的原子轨道数为_____________个,氧、硫、氯的第一电离能由大到小顺序为________________。
(2)SCl2分子中的中心原子杂化轨道类型是_____________,该分子空间构型为__________。
(3)第四周期中,与氯原子未成对电子数相同的金属元素有_______种。
(4)晶体硅的结构与金刚石非常相似。金刚石、晶体硅和金刚砂(碳化硅)的熔点由高到低的顺序为____________(填化学式)。
(5)下表是一组物质的沸点数据:
有机物 | 甲醇(CH3OH) | 丙烯(CH3CH=CH2) | 一氟甲烷(CH3F) |
相对分子质量 | 32 | 42 | 34 |
沸点/℃ | 64.7 | -47.7 | -78.2 |
若只考虑相对分子质量,甲醇沸点应低于-78.2℃,甲醇沸点高的原因是________。
丙烯中含有的α键与π键个数之比为______________。
(6)铝单质为面心立方晶体,其晶胞结构如图,晶胞参数qcm,铝的摩尔质量为Mg·mol-1,原子半径为r pm,阿伏伽德罗常数的值为NA,该晶体的空间利用率为_______________(只要求列算式,不必计算出数值)。

【题目】在一定温度下,10mL 0.40mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A. 0~6 min的平均反应速率:v(H2O2)≈ 3.3×10﹣2 mol/(Lmin)
B. 6~10 min的平均反应速率:v(H2O2)< 3.3×10﹣2 mol/(Lmin)
C. 反应到6 min时,H2O2分解了50%
D. 反应到6 min时,c(H2O2)=0.30 mol/L