题目内容
【题目】由醇X制备羧酸Z的合成路线如图所示,不正确的是( )

A. Y的结构有4种
B. X、Z能形成戊酸丁酯,戊酸丁酯最多有16种
C. 与X互为同分异构体,且不能与金属钠反应的有机物有4种
D. 与Z互为同分异构体,且能发生水解反应的有机物有9种
【答案】C
【解析】
A、丁基有四种结构:![]()
![]() ,Y是丁基和溴原子结合而成,所以有四种结构,选项A正确;
,Y是丁基和溴原子结合而成,所以有四种结构,选项A正确;
B、戊酸丁酯中的戊酸,相当于丁基连接一个—COOH,所以有四种结构,而丁醇是丁基连接一个—OH,所以也有四种结构,因此戊酸丁酯最多有16种,选项B正确;
C、X为丁醇,其同分异构体中不能与金属钠反应的是醚,分别是C—O—C—C—C、C—C—O—C—C和![]() 共3种,选项C不正确;
共3种,选项C不正确;
D、Z是戊酸,其同分异构体能发生水解的属于酯类,HCOOC4H9有4种,CH3COOC3H7有2种,CH3CH2COOCH2CH3、CH3CH2CH2COOCH3、(CH3)2CHCOOCH3,所以共9种,选项D正确。
答案选C。

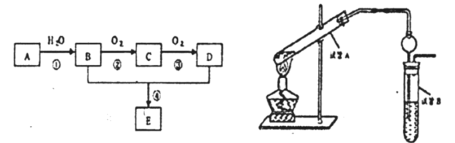
【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
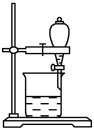
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O