��Ŀ����
����Ŀ����֪�о������仯�����ת�����ڻ����������ش����塣
I����֪N2(g) +O2(g)=2NO(g) ��H=+180.4 kJ/mol��
4NH3(g)+5O2(g)=4NO(g)+6H2O��l�� ��H=![]() kJ/mol��
kJ/mol��
(1)��NH3����NO��Ⱦ�ķ�ӦΪ��4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) ��H=_______����÷�Ӧ�Է����е�������______________(����¡����¡�)��
5N2(g)+6H2O(l) ��H=_______����÷�Ӧ�Է����е�������______________(����¡����¡�)��
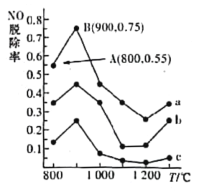
(2)��ͬ�¶������£�NH3��NO�����ʵ���֮�ȷֱ�Ϊ4:1��3:1��1:3���õ�NO�ѳ���������ͼ��ʾ������a��NH3����ʼŨ��Ϊ4��10- 5mol/L����A�㵽B�㾭��2�룬��ʱ�����NO���ѳ�����Ϊ_______mg/��L��s������AB���ڵ������ϵ��¶ȸ���900��ʱNO�ѳ������Խ��͵�ԭ����_______________________________________________��
��.�û���̼��ԭ��Ҳ���Դ�����������������ķ�ӦΪ2CO(g)+ 2NO(g)![]() N2(g)+2CO2(g) ��H=-746.8kJ/mol��
N2(g)+2CO2(g) ��H=-746.8kJ/mol��
(3)��һ���ݾ��ȵ��ܱ������У��ܱ�ʾ������Ӧ�ﵽƽ��״̬����_____________(����ĸ����)��
A����λʱ���ڶ���1 mol N��N����ͬʱ����2 mol C=O��
B�������ڵ���ѹǿ���ֲ���
C�����������ܶȱ��ֲ���
D��c(NO):c(N2):c(CO2)=2:1:2
E����������ƽ��Ħ���������ֲ���
(4)��һ�����ܱ������г���3mol CO��2mol NO������������ѹΪ10MPa����һ���¶��¿�ʼ��Ӧ��10 min��ﵽƽ�⣬���NO��ת����Ϊ75%���÷�Ӧ��ƽ�ⳣ��KP=____________����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�����������
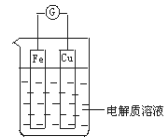
���ü�ӵ绯ѧ���ɶԴ�����Ⱦ��NO���������������乤��ԭ����ͼ��ʾ������Ĥ����H+��H2Oͨ����
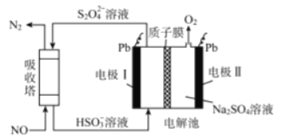
(5)д���������е����ӷ�Ӧ����ʽ_____________________________________����Ӧ��������ͨ�����ӽ���Ĥ��H+Ϊ1 molʱ�������������ɵ������ڱ�״���µ����Ϊ_____ L��
���𰸡�-1807.8 kJ/mol ���� 0.03 �÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���NO�ѳ��ʽ��� BE 1.5MPa-1 2NO+2S2O42-+2H2O=N2+4HSO3- 5.6
��������
I��(1)���ݸ�˹���ɽ��м��㲢�жϣ����ݸ����оݽ��з�Ӧ����������
(2) ����a��NH3����ʼŨ��Ϊ4��10- 5mol/L������ͼ��õ�A��B������NO�ѳ��ʣ��ɵ�����NO��Ũ�ȣ��������ѳ����ʣ����Ĵ�������Ӧ�Ƿ��ȷ�Ӧ���ݴ˽��з����жϣ�
��. (3)�ﵽƽ��״̬ʱ������Ӧ�������淴Ӧ������ȣ������ʵ�������Ũ�ȱ��ֲ��䣬�ݴ˽��з����жϣ�
(4)����NO��ת����Ϊ75%���ɼ���õ�NOת�������ʵ�������һ���ɼ����ƽ��ʱ�����ʵ����ʵ��������������ʵ����Ĺ�ϵ�ɵ�ƽ��ʱ����ѹ��������÷�ѹ=��ѹ�����ʵ�����������������ʵķ�ѹ���Ӷ��õ�ƽ�ⳣ����
��(5)��������ͨ���NO��S2O42-������Ӧ������N2��HSO3-���ݴ���д���ӷ���ʽ�����ص����������ĵ缫��ӦΪ��2H2O-4e-=4H++O2������ת��1mol����ʱ����4molH+ͨ�����ӽ���Ĥ���ɴ˽��м��㣻
I��(1)�� N2(g) +O2(g)=2NO(g) ��H1=+180.4 kJ/mol����4NH3(g)+5O2(g)=4NO(g)+6H2O��H2=![]() kJ/mol�����ݸ�˹���ɿ�֪��H=��H2-5��H1=
kJ/mol�����ݸ�˹���ɿ�֪��H=��H2-5��H1=![]() kJ/mol-5��(+180.4 )kJ/mol=-1807.8 kJ/mol�����ݸ����оݿ�֪��H<0,S<0���÷�Ӧ�Է����е������ǵ��£�
kJ/mol-5��(+180.4 )kJ/mol=-1807.8 kJ/mol�����ݸ����оݿ�֪��H<0,S<0���÷�Ӧ�Է����е������ǵ��£�
(2) ����a��NH3����ʼŨ��Ϊ4��10- 5mol/L����ôNO����ʼŨ��Ϊ1��10- 5mol/L��A����ѳ���Ϊ55%��B����ѳ���Ϊ75%����A�㵽B�㾭��2�룬�ö�ʱ����NO���ѳ�����Ϊ![]() =0.03 mg/��L��s������AB���ڵ������ϵ��¶ȸ���900��ʱNO�ѳ������Խ��͵�ԭ���Ǹ÷�ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�������ƶ������NO�ѳ��ʽ��ͣ�
=0.03 mg/��L��s������AB���ڵ������ϵ��¶ȸ���900��ʱNO�ѳ������Խ��͵�ԭ���Ǹ÷�ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�������ƶ������NO�ѳ��ʽ��ͣ�
��. (3) A����λʱ���ڶ���1 mol N��N����ͬʱ����2 mol C=O����ֻ������Ӧ��û������Ӧ����ȷ������Ӧ�������淴Ӧ������ȣ���˲���֤���ﵽƽ��״̬��A�����
B���÷�ӦΪ�����С�ķ�Ӧ���������ڵ���ѹǿ���ֲ���ʱ��˵���ﵽ��ƽ��״̬��B����ȷ��
C���ں�����ϵ�У���Ӧǰ���������������䣬���Ի��������ܶ�ʼ�ձ��ֲ��䣬����֤���÷�Ӧ�ﵽƽ��״̬��C�����
D����c(NO):c(N2):c(CO2)=2:1:2ʱ����Ӧ��һ���ﵽƽ��״̬���뷴Ӧ��ʼŨ�ȼ�ת�����йأ�����֤���÷�Ӧ�ﵽƽ��״̬��D�����
E���÷�ӦΪ�ǵ������Ӧ������������ƽ��Ħ���������ֲ���ʱ����֤���÷�Ӧ�ﵽ��ƽ��״̬��E����ȷ��
��ѡBE��
(4) ����NO��ת����Ϊ75%����֪NOת�������ʵ���Ϊ1.5mol������
2CO(g)+ 2NO(g)![]() N2(g)+ 2CO2(g)
N2(g)+ 2CO2(g)

ƽ��ʱ����ѹΪ10 MPa��![]() =8.5 Mpa
=8.5 Mpa
��ôKP=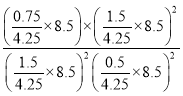 =1.5 MPa-1��
=1.5 MPa-1��
��(5) ��������ͨ���NO��S2O42-������Ӧ������N2��HSO3-�����ӷ���ʽΪ��2NO+2S2O42-+2H2O=N2+4HSO3-�����ص����������ĵ缫��ӦΪ��2H2O-4e-=4H++O2������ת��4mol����ʱ����4molH+ͨ�����ӽ���Ĥ����˵�ͨ�����ӽ���Ĥ��H+Ϊ1 molʱ������������ʵ���Ϊ0.25mol���������������ɵ������ڱ�״���µ����Ϊ0.25mol��22.4L/mol=5.6L��