题目内容
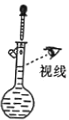
【题目】如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.

(1)指出图中明显的错误________________;________________;
(2)A仪器的名称是________________;B仪器的名称是________________;
(3)萃取、分液实验中所用主要玻璃仪器的名称是________________,静置后分液的第一步操作是________________。
【答案】温度计插入蒸馏烧瓶中部的位置 冷凝管中自来水进入的方向 蒸馏烧瓶 冷凝管 分液漏斗 打开分液漏斗上端活塞
【解析】
(1)根据装置图可知温度计水银球应处在蒸馏烧瓶的支管口附近,用来测量蒸汽的温度,冷凝管应从下口进水,上口出水,以保证水充满冷凝管,起到充分冷凝的作用;因此错误是温度计插入蒸馏烧瓶中部的位置、冷凝管中自来水进入的方向;
(2)根据仪器构造可知A仪器的名称是蒸馏烧瓶,B仪器的名称是冷凝管;
(3)萃取、分液实验中所用主要玻璃仪器的名称是分液漏斗,要想实现分液操作,静置后应先打开分液漏斗上端活塞使瓶内外气压相等,然后下层液体从下端放出,上层液体从上口倒出。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】依据下表25℃时某些弱酸的电离平衡常数,判断下列说法正确的是
CH3COOH | HC1O | H2CO3 |
Ka=1.8×l0-5 | Ka=3.0×l0-8 | Ka1=4.4×l0-7 Ka2=4.7×l0-11 |
A. 向NaClO溶液中通入少量CO2的离子方程式为:2C1O-+CO2+H2O==2HC1O+CO32-
B. 相同浓度的CH3COOH和NaClO的溶液中,水的电离程度前者大
C. 向0. lmol L-l的CH3COOH溶液中滴加NaOH溶液至pH = 5,此时溶液的 c(CH3COOH):c(CH3COO-) =5∶9
D. 常温下,0 lmol L-1 的 NaHC2O4 溶液 pH =4: c(HC2O4-) >c(H+)>c(H2C2O4)>c(C2O42-)
【题目】含氮化合物在化学工业中有着重要的应用,回答下列问题:
(1)由N2O和NO反应生成N2和NO2的能量变化(表示生成1molN2的能量变化)如图所示,该反应的热化学方程式为______________________。

(2)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=___________;若有1mol硝酸铵完全分解,则转移电子的数目为___________(设NA为阿伏加德罗常数的值)。
(3)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH-![]() O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
t/s | 0 | 60 | 90 | 120 | 160 | 260 | 300 | 360 | 400 |
a/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
①该反应在60~90s与90~120s内的平均反应速率分别约为___________,___________;比较两者大小可得出的结论是______________________。
②计算T℃时该反应的平衡常数为______________________。
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为______________________(写出一条即可)。