题目内容
【题目】混合物的分离提纯在生产生活中有着重要的意义,请根据题目要求完成下题:
已知某工业废水中含有大量FeSO4,较多的Cu2+,以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。
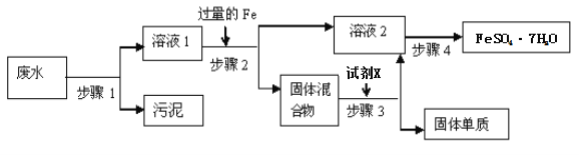
(1)步骤1的主要操作中需用到的玻璃仪器有____,____,_____。
(2)步骤2中发生反应的离子方程式为_____。
(3)步骤3中加入的试剂X为_____。
(4)步骤4中涉及的操作是:蒸发浓缩、___、过滤、洗涤、烘干。
【答案】漏斗 玻璃棒 烧杯 Fe+Cu2+=Fe2++Cu 稀硫酸 冷却结晶或降温结晶
【解析】
工业废水中含有大量FeSO4,较多的Cu2+,以及部分污泥,首先通过步骤1进行过滤除去污泥,在步骤2中加入过量的Fe,发生Fe+Cu2+=Fe2++Cu,过量的Fe用稀硫酸除去,发生反应为![]() ,最后所得滤液经蒸发浓缩、冷却结晶、过滤可得到FeSO4·7H2O晶体。
,最后所得滤液经蒸发浓缩、冷却结晶、过滤可得到FeSO4·7H2O晶体。
(1)步骤1、步骤2、步骤3都为过滤操作,需要的玻璃仪器有烧杯、玻璃棒、普通漏斗,
故答案为:漏斗、玻璃棒、烧杯;
(2)在步骤2中加入过量的Fe,发生Fe+Cu2+=Fe2++Cu,以制得单质Cu,
故答案为:Fe+Cu2+=Fe2++Cu;
(3)经步骤2后所得固体混合物为Fe和Cu的混合物,过量的Fe用稀硫酸除去,
故答案为:稀硫酸;
(4)最后所得滤液经蒸发浓缩、冷却结晶、过滤可得到FeSO4·7H2O晶体,
故答案为:冷却结晶或降温结晶。

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目