题目内容
【题目】有H2SO4和HNO3的混合溶液20 mL,加入0.25 molL﹣1Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液呈中性)。则原混合液中H2SO4的物质的量浓度为__mol·L-1,HNO3的物质的量浓度为__mol·L-1。

【答案】0.25 1
【解析】
由图可知,加入20mLBa(OH)2溶液时,硫酸钡沉淀达最大值,故根据方程式计算硫酸的物质的量;由图可知,pH=7时,消耗60mLBa(OH)2溶液,由H++OH-═H2O可知n(H+)=n(OH-),据此计算原溶液中含有的n(H+),进而计算硝酸的电离产生的氢离子物质的量,再根据c=![]() 计算硫酸、硝酸的物质的量浓度。
计算硫酸、硝酸的物质的量浓度。
由图可知,0~20 mL Ba(OH)2溶液发生H2SO4+Ba(OH)2=BaSO4↓+H2O,20~60 mL Ba(OH)2溶液发生发生H++OH﹣=H2O;
加入20 mL Ba(OH)2溶液时,硫酸钡沉淀达最大值,设硫酸的物质的量为x,则:
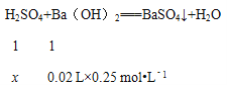
故x=0.02 L×0.25 molL﹣1=0.005 mol,
硫酸的物质的量浓度为![]() =0.25 molL﹣1,
=0.25 molL﹣1,
由图可知,pH=7时,消耗60 mL Ba(OH)2溶液,由H++OH﹣=H2O可知原溶液中含有的n(H+)=n(OH﹣)=2×0.06 L×0.25 molL﹣1=0.03 mol,故n(HNO3)=0.03 mol-0.005 mol×2=0.02 mol;
故原溶液中HNO3的物质的量浓度=![]() =1 mol·L-1。
=1 mol·L-1。

 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】在一定温度下,10mL 0.40mol/L H2O2 溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:υ(H2O2)=3.3×10-2mol/(L·min)
B.6~10min的平均反应速率:υ(H2O2)<3.3×10-2mol/(L·min)
C.反应到6min时,c(H2O2)=0.30mol/L
D.反应到6min时,H2O2 分解了50%