题目内容
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的3倍 ,下列说法中不正确的是( )
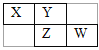
A. 单质Y的氧化性强于X
B. Y和Z具有相同的最高正化合价
C. W的单质常温呈气态
D. X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐
【答案】B
【解析】
Y原子的最外层电子数是次外层电子数的3倍,则Y是O元素;根据X、Y、Z、W在周期表中的相对位置,可知X、Z、W分别是N、S、Cl元素。
A. 同周期元素从左到右非金属性增强,单质氧化性增强,所以氧气的氧化性强于氮气,故A正确;
B. 氧元素的最高价不是+6,S元素的最高正化合价是+6,故B错误;
C. W是氯元素,氯气常温呈气态,故C正确;
D. N的气态氢化物是氨气,N的最高价氧化物对应的水化物是硝酸,氨气和硝酸反应生成硝酸铵,故D正确。选B。

【题目】按要求回答问题:
(1)KAl(SO4)2的电离方程式_________。
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是_________、_________ (填微粒符号)。
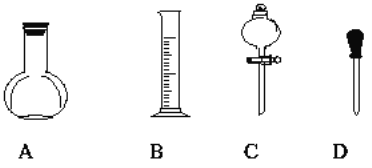
(3)实验室需配制0.5mol/L的硫酸溶液480mL,在下图所示仪器中,配制上述溶液肯定不需要的是___(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是________。
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L(标况)SO2时,转移的电子是__________mol。
(5)下列四个图像中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。
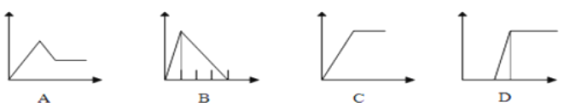
溶液 | 加入的物质 | 序号 |
①AlCl3溶液 | 通入过量的NH3 | ___ |
②Na2CO3和NaOH的溶液 | 滴入过量的盐酸 | ___ |
③NaAlO2溶液 | 滴加稀硫酸至过量 | __ |
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为______nm。
所形成的正八面体的体心,该正八面体的边长为______nm。