题目内容
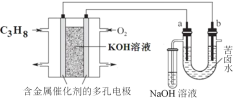
【题目】用碱性丙烷燃料电池电解苦卤水(含Cl、Br、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是
A.电池工作时,负极反应式为:C3H8+26OH20e![]() 3
3![]() +17H2O
+17H2O
B.电解时,a电极周围首先放电的是Br而不是Cl,说明当其他条件相同时后者的还原性强于前者
C.电解时,电子流动的路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量损耗,当电池中消耗 0.16 g O2时,a极周围会产生0.71 g Cl2
【答案】A
【解析】本题考查原电池和电解池的原理,需要掌握几种燃料电池分别在酸性条件或碱性条件下电极反应的书写。左边能自发的进行氧化还原反应,为原电池,氧气得电子发生还原反应,则通入氧气的电极为正极,丙烷为负极,右边是电解池,a为阳极,b为阴极,原电池工作时,丙烷燃料电池,以氢氧化钾为电解质,总反应为C3H8+5O2+6OH![]() 3
3![]() +7H2O,正极为O2+2H2O +4e
+7H2O,正极为O2+2H2O +4e![]() 4OH(还原反应),负极C3H8+26OH20e
4OH(还原反应),负极C3H8+26OH20e![]() 3
3![]() +17 H2O (氧化反应),故A正确,B.还原性强的离子在阳极先放电,电解时,a电极周围首先放电的是Br而不是Cl,所以还原性是溴离子的还原性强于氯离子,故B错误。C.电子在导线中移动,不能在溶液中移动,电解时,电子流动路径是:负极→外电路→阴极,阳极→外电路→正极,故C错误,D.若苦卤水只有氯离子,根据转移电子相等可知,当电池中消耗0.16 g氧气时,理论上阳极上可以产生0.71 g氯气,但溶液中有溴离子,溴离子首先发生放电,然后到氯离子放电,所以氯气的量应该小于0.71 g,故D错误。答案选AB。
+17 H2O (氧化反应),故A正确,B.还原性强的离子在阳极先放电,电解时,a电极周围首先放电的是Br而不是Cl,所以还原性是溴离子的还原性强于氯离子,故B错误。C.电子在导线中移动,不能在溶液中移动,电解时,电子流动路径是:负极→外电路→阴极,阳极→外电路→正极,故C错误,D.若苦卤水只有氯离子,根据转移电子相等可知,当电池中消耗0.16 g氧气时,理论上阳极上可以产生0.71 g氯气,但溶液中有溴离子,溴离子首先发生放电,然后到氯离子放电,所以氯气的量应该小于0.71 g,故D错误。答案选AB。

练习册系列答案
相关题目



