题目内容
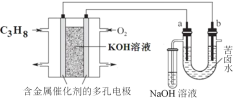
【题目】如图甲是一种利用微生物将废水中的尿素(H2NCONH2,氮元素显3价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是

A.H+透过质子交换膜由右向左移动
B.铜电极应与X相连接
C.M电极的反应式:H2NCONH2+H2O6e![]() CO2↑+N2↑+6H+
CO2↑+N2↑+6H+
D.当N电极消耗0.5 mol气体时,则铁电极增重32 g
【答案】C
【解析】本题考查了原电池、电解池原理的应用。由图甲O2生成H2O ,可知N为正极,M为负极;在原电池中阳离子向正极移动,所以H十应移向正极,由左向右移动,故A错;利用此装置的电能在铁上镀铜,则铜电极失电子为阳极,与电源正极相连,所以铜电极应与Y相连接,故B错;尿素失电子生成CO2和N2,碳元素化合价没有变化,1 mol尿素失去6 mol电子,再根据原子守恒和电荷守恒可得M电极的反应式:H2NCONH2+H2O6e![]() CO2↑+N2↑+6H+,故C正确;N电极为氧气得电子生成水,电极反应式为O2+4e+4H+
CO2↑+N2↑+6H+,故C正确;N电极为氧气得电子生成水,电极反应式为O2+4e+4H+![]() 2H2O,由电极反应式可知,N电极消耗0.5 mol氧气时,转移2 mol电子,则铁电极析出1 mol铜,质量增重应为64 g,故D错。
2H2O,由电极反应式可知,N电极消耗0.5 mol氧气时,转移2 mol电子,则铁电极析出1 mol铜,质量增重应为64 g,故D错。

【题目】下述实验能到达预期目的的是
选项 | 实验内容 | 实验目的 |
A | 用注射器收集铜与浓硝酸反应生成的气体,然后推拉注射器 | 研究压强对化学平衡移动的影响 |
B | 在实验室制得的乙酸乙酯中加入饱和碳酸钠溶液,然后蒸馏 | 除去乙酸乙酯中混有的乙酸、乙醇 |
C | 用饱和FeCl3溶液制得Fe(OH)3胶体,然后过滤 | 提纯Fe (OH) 3胶体 |
D | 往混有FeCl2的CuCl2溶液中加人H2O2 后,用氨水调节pH 至2.7 后过滤 | 除去CuCl2溶液中FeCl2杂质 |
A. A B. B C. C D. D
【题目】某小组以醋酸为例探究弱酸的性质。
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响。
①设计实验方案如下表,表中c =________ mol·L-1。
编号 | 酸的种类 | 酸的浓度/mol·L-1 | 酸的体积/mL | 镁条质量/g |
1 | 醋酸 | 1.0 | 10 | 2.0 |
2 | 盐酸 | c | 10 | 2.0 |
②实验步骤:a)检查装置(左图)的气密性后,添加药品;
b)反应开始后,___________________________(填写操作) ;
c)将所记录的数据转化为曲线图(右图)。

③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:____________。
(2)实验二:现有一瓶醋酸溶液,常温下测定其中醋酸的电离程度(已电离的电解质分子数占原来总分子数的百分比)。
设计实验方案,将待测物理量和对应的测定方法填写在下表中。
待测物理量 | 测定方法 |
①__________ | 量取25.00mL醋酸溶液于锥形瓶中,滴加指示剂,将0.1000 mol·L-1 NaOH标准溶液装入______________中,滴定至终点,记录数据.重复滴定2次. |
②__________ | _______________________________________ |