题目内容
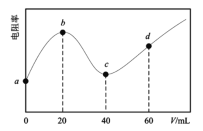
【题目】298K时,向20mL均为0.1mol·L-1的MOH和NH3·H2O混合液中滴加0.1mol·L-1的CH3COOH溶液,测得混合液的电阻率(表示电阻特性的物理量)与加入CH3COOH溶液的体积(V)的关系如图所示。已知:CH3COOH的Ka=l.8×10-5,NH3H2O的Kb=l.8×l0-5。下列说法错误的是( )
A.碱性:MOH>NH3·H2O
B.c点溶液中浓度:c(CH3COOH)>c(NH3H2O)
C.d点溶液的pH≈5
D.a→d过程中水的电离程度先减小后增大
【答案】D
【解析】
溶液中离子浓度越小,溶液的导电率越小,电阻率越大;a→b过程中随着CH3COOH的滴入,电阻率增大,b点达最大,说明a→b过程中随着CH3COOH的滴入离子浓度减小,而CH3COOH滴定氨水时生成的CH3COONH4是强电解质,溶液的导电性应增大,故向混合溶液中加入等物质的量浓度的CH3COOH溶液时,发生反应的先后顺序是MOH+CH3COOH= CH3COOM+H2O、NH3·H2O+ CH3COOH= CH3COONH4+H2O,则碱性MOH>NH3·H2O,b点溶液中溶质为CH3COOM、NH3·H2O,c点时醋酸和氨水恰好完成反应生成醋酸铵,c点溶液中溶质为CH3COOM,CH3COONH4且二者的物质的量浓度相等。
A. 由图可知,向混合溶液中加入等物质的量浓度的CH3COOH溶液时,电阻率先增大后减小,说明发生了两步反应,发生反应先后顺序是碱性强的MOH先反应MOH+CH3COOH= CH3COOM +H2O,然后NH3·H2O+ CH3COOH= CH3COONH4+H2O,所以碱性MOH>NH3·H2O,故A正确;
B. c点时,加入醋酸40mL时,溶液中的溶质为CH3COOM、CH3COONH4且二者的物质的量浓度相等,又因为CH3COOH的Ka=1.8×10-5等于NH3·H2O的Kb=1.8×10-5,CH3COONH4溶液呈中性,又碱性:MOH>NH3·H2O,CH3COOM溶液呈碱性,c点溶液呈碱性,则醋酸根的水解程度大于铵根的水解程度,则c(CH3COOH)>c(NH3·H2O),故B正确;
C. d点加入醋酸60mL,溶液中的溶质为CH3COOM、CH3COONH4和CH3COOH且三者物质的量浓度相等,由于盐的水解程度和弱酸的电离程度都是微弱的,则c(CH3COO-)≈2c(CH3COOH),由醋酸的电离常数Ka=![]() = l.8×10-5可知c(H+)≈ 9×10-6mol/L,则溶液pH≈5,故C正确;
= l.8×10-5可知c(H+)≈ 9×10-6mol/L,则溶液pH≈5,故C正确;
D. a→d过程,溶液的碱性逐渐减弱,水电离程度加大,后来酸性逐渐增强,水的电离程度减小,所以实验过程中水的电离程度是先增大后减小,故D错误;
故选D。

 名校课堂系列答案
名校课堂系列答案