题目内容
化学中常用图像直观地描述化学反应的进程或结果。下列对图像描述叙述正确的是
A.根据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)的△H>0 2AB3(g)的△H>0 |
B.图②表示压强对可逆反应2A(g)+B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.据图④,若除去0.1mol·L-1CuSO4溶液中的Fe3+可向溶液中加入适量NaOH至pH约为5 |
B
解析试题分析:A、根据图①可知,反应速率曲线交点之前,反应未达平衡,交点时处于平衡状态。交点后升高温度逆反应速率增大比正反应速率增大的更多,说明平衡向逆反应移动。由于升高温度平衡向吸热反应方向移动,故可判断可逆反应A2(g)+3B2(g) 2AB3(g)正反应是放热反应,即△H<0,所以A错误;B、由图②可知,由甲到乙,到达平衡时间缩短,说明条件改变使乙的反应速率加快,但平衡时反应物的转化率不变,即改变条件平衡不移动,对可逆反应2A(g)+B(g)
2AB3(g)正反应是放热反应,即△H<0,所以A错误;B、由图②可知,由甲到乙,到达平衡时间缩短,说明条件改变使乙的反应速率加快,但平衡时反应物的转化率不变,即改变条件平衡不移动,对可逆反应2A(g)+B(g) 3C(g)+D(s)来说,反应前后体积体积不变,所以增大压强平衡不移动,故B正确;C、乙酸是弱酸,存在电离平衡。乙酸溶液中通入氨气生成乙酸铵,由弱电解质变为强电解质,溶液的导电能力增强,到达最大值后,导电能力几乎不变,与图象不相符,故C错误;D、由图可知,Fe3+在pH=4左右沉淀完全,此时铜离子不沉淀,故可以加入适量NaOH,调节pH在4左右,除去CuSO4溶液中的Fe3+。当pH=5时,铜离子开始形成沉淀,故D错误,答案选B。
3C(g)+D(s)来说,反应前后体积体积不变,所以增大压强平衡不移动,故B正确;C、乙酸是弱酸,存在电离平衡。乙酸溶液中通入氨气生成乙酸铵,由弱电解质变为强电解质,溶液的导电能力增强,到达最大值后,导电能力几乎不变,与图象不相符,故C错误;D、由图可知,Fe3+在pH=4左右沉淀完全,此时铜离子不沉淀,故可以加入适量NaOH,调节pH在4左右,除去CuSO4溶液中的Fe3+。当pH=5时,铜离子开始形成沉淀,故D错误,答案选B。
考点:考查外界条件对反应速率和平衡状态影响;电解质的电离平衡以及溶液导电性判断;难溶电解质的溶解平衡以及沉淀形成时pH控制等

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案已知反应2D+E 3F+2G,用传感器测得该反应在不同pH条件下,物质D的浓度(用每升溶液所含溶质的质量表示,单位为mg/L)变化如图所示,下列有关说法正确的是
3F+2G,用传感器测得该反应在不同pH条件下,物质D的浓度(用每升溶液所含溶质的质量表示,单位为mg/L)变化如图所示,下列有关说法正确的是
| A.pH=6.8时,D的浓度(mg/L)一定最大 |
| B.在pH相同的条件下,增大压强,D的浓度(mg/L)增大 |
| C.调节pH到8.8,可使该反应正、逆反应速率都为0 |
| D.温度相同时,不同pH条件下,该反应的平衡常数相同 |
在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1)
2NH3(g) △H=-92.4 kJ·mol-1)
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1 mol N2、3 mol H2 | 4 mol NH3 |
| NH3的浓度(mol·L-1) | c1 | c2 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ |
| 气体密度 | ρ1 | ρ2 |
| 反应物转化率 | α1 | α2 |
下列说法正确的是
A.c1<c2<2 c1 B.a+b>92.4 C.α1 +α2=1 D.ρ2=2ρ1
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3-(aq);某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法中不正确的是( )
I3-(aq);某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法中不正确的是( )
A.反应I2(aq)+I-(aq) I3-(aq)的△H<0 I3-(aq)的△H<0 |
| B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2 |
| C.若反应进行到状态D时,一定有v正<v逆 |
| D.状态A与状态B相比,状态B的c(I2)大 |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。 向其中一份中逐渐加入铜粉,最多能溶解19.2 g。向另一份中逐渐 加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是( )
| A.原混合酸中NO3-物质的量浓度为2 mol/L |
| B.OA段产生的是NO,AB段的反应为 Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
下列说法正确的是
| A.除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤 |
| B.某温度时,纯水中c(H+)=2×10-7mol·L-1,则c(OH-)=5×10-8mol·L-1 |
C.N2(g)+3H2(g) 2NH3(g),其他条件不变,增大压强,v(正)增大而v(逆)减小 2NH3(g),其他条件不变,增大压强,v(正)增大而v(逆)减小 |
D.Na2CO3溶液中存在平衡:CO32-+H2O HCO3-+OH一,升高温度溶液碱性增强 HCO3-+OH一,升高温度溶液碱性增强 |
在一固定容积的密闭容器中进行如下反应:2SO (g)+O
(g)+O (g)
(g) 2SO
2SO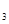 (g),已知反应进行到10秒时,SO
(g),已知反应进行到10秒时,SO 、O
、O 、SO
、SO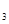 的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
A.10秒时,用O 表示该反应的平均反应速率为0.01 mol/(L·s) 表示该反应的平均反应速率为0.01 mol/(L·s) |
B.当反应达平衡时,SO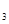 的物质的量可能为0.4 mol 的物质的量可能为0.4 mol |
C.当SO 和O 和O 的生成速率之比为2:1时,达到该反应限度 的生成速率之比为2:1时,达到该反应限度 |
D.向容器内充人SO ,可以提高反应速率 ,可以提高反应速率 |
 2C(g),根据下表中的数据判断下列图像错误的是
2C(g),根据下表中的数据判断下列图像错误的是

 2SO2(g)+O2(g)
2SO2(g)+O2(g)