题目内容
下列叙述正确的是( )
| A、48g O3和O2的混合气体中含有6.02×1023个分子 |
| B、常温常压下,4.6g NO2气体含有1.806×1023个原子 |
| C、0.5mol?L-1 1L CuCl2溶液中含有3.01×1023个Cu2+ |
| D、标准状况下,3.36L H2O含有9.03×1023个分子H2O |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.臭氧和氧气的摩尔质量不同,无法计算48g混合气体的物质的量及分子数;
B.4.6g二氧化氮的物质的量为0.1mol,根据质量守恒,含有的原子的物质的量为0.3mol;
C.氯化铜溶液中,铜离子部分水解,溶液中铜离子的数目减少;
D.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量.
B.4.6g二氧化氮的物质的量为0.1mol,根据质量守恒,含有的原子的物质的量为0.3mol;
C.氯化铜溶液中,铜离子部分水解,溶液中铜离子的数目减少;
D.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量.
解答:
解:A.48g臭氧的物质的量为1mol,48g氧气的物质的量为1.5mol,所以48g臭氧和氧气的物质的量大于1mol,含有的电子数大于6.02×1023,故A错误;
B.4.6gNO2气体的物质的量为0.1mol,根据质量守恒定律,0.1mol二氧化氮中一定含有0.1mol氮原子和0.2mol氧原子,总共含有0.3mol原子,含有的原子数为1.806×1023,故B正确;
C.0.5mol?L-1 1L CuCl2溶液中含有溶质氯化铜0.5mol,铜离子部分水解,溶液中铜离子的物质的量小于0.5mol,溶液中含有的铜离子数目小于3.01×1023,故C错误;
D.标准状况下,水不是气体,题中条件无法计算水的物质的量,故D错误;
故选B.
B.4.6gNO2气体的物质的量为0.1mol,根据质量守恒定律,0.1mol二氧化氮中一定含有0.1mol氮原子和0.2mol氧原子,总共含有0.3mol原子,含有的原子数为1.806×1023,故B正确;
C.0.5mol?L-1 1L CuCl2溶液中含有溶质氯化铜0.5mol,铜离子部分水解,溶液中铜离子的物质的量小于0.5mol,溶液中含有的铜离子数目小于3.01×1023,故C错误;
D.标准状况下,水不是气体,题中条件无法计算水的物质的量,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下水、四氯化碳、乙醇等不是气体,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项C为易错点,注意铜离子部分水解.

练习册系列答案
相关题目
下列物质中既能与NaOH溶液反应,又能与稀硫酸反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3 ⑥(NH4)2CO3.
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3 ⑥(NH4)2CO3.
| A、②③④⑤ | B、②③④⑥ |
| C、①②③④⑤ | D、①②③④⑥ |
下列说法正确的是( )
| A、变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 |
| B、因为NaCl的水溶液能导电,所以NaCl溶液属于强电解质 |
| C、铝合金的大量使用是因为人们能用焦炭等还原剂从氧化铝中获取铝 |
| D、37Cl 是氯元素的一种核素,37Cl的中子数和电子数之差是3 |
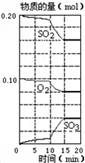 在一定条件下,二氧化硫和氧气发生如下反应:
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2 (g)?2SO3(g);△H<0.
600℃时,在某密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量有如图所示的变化.其中10min到15min时,与图象相符的变化是( )
| A、加了催化剂 |
| B、增加SO3的物质的量 |
| C、升高温度 |
| D、缩小容器体积 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、常温常压下,4g CH4含NA个共价键 |
| B、常温常压下,22.4L氦气含有的原子数为2NA |
| C、1mol S在足量O2中燃烧,转移的电子数为6NA |
| D、0.1mol?L-1的碳酸氢钠溶液中含钠离子数为0.1NA |
将51.2g铜恰好完全溶于一定量的硝酸溶液中,得到硝酸铜溶液,收集到氮的氧化物(含NO、NO2、N2O4)的混合物共17.92L(标准状况),在这些气体中通入V L(标准状况)的氧气后用一定量的氢氧化钠溶液吸收,结果剩余2.24L(标准状况)气体.则通入氧气的体积V为( )
| A、7.28L |
| B、8.96L |
| C、11.20L |
| D、16.8L |
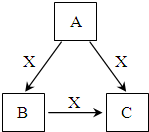 A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示的转化关系(其他产物已略去),下列说法不正确的是( )
A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示的转化关系(其他产物已略去),下列说法不正确的是( )| A、若X为O2,则A可能是金属单质,也可能是非金属单质 |
| B、若X为O2,则A可能是化合物 |
| C、若X为NaOH溶液,则A可能是化合物 |
| D、若X为NaOH溶液,则A可能为单质 |