题目内容
 在一定条件下,二氧化硫和氧气发生如下反应:
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2 (g)?2SO3(g);△H<0.
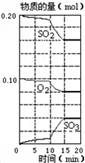
600℃时,在某密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量有如图所示的变化.其中10min到15min时,与图象相符的变化是( )
| A、加了催化剂 |
| B、增加SO3的物质的量 |
| C、升高温度 |
| D、缩小容器体积 |
考点:二氧化硫的化学性质
专题:氧族元素
分析:10min到15min时,SO2、O2的物质的量减小,且减少的量为2:1,SO3物质的量增大,则改变条件使平衡正向移动,以此来解答.
解答:
解:10min到15min时,SO2、O2的物质的量减小,且减少的量为2:1,SO3物质的量增大,则改变条件使平衡正向移动,
A.催化剂对平衡移动无影响,故A不选;
B.增加SO3的物质的量平衡逆向移动,SO2、O2的物质的量增大,故B不选;
C.△H<0为放热反应,升高温度平衡逆向移动,故C不选;
D.2SO2(g)+O2 (g)?2SO3(g)为气体体积减小的反应,则缩小容器体积,压强增大平衡正向移动,与图一致,故D选;
故选D.
A.催化剂对平衡移动无影响,故A不选;
B.增加SO3的物质的量平衡逆向移动,SO2、O2的物质的量增大,故B不选;
C.△H<0为放热反应,升高温度平衡逆向移动,故C不选;
D.2SO2(g)+O2 (g)?2SO3(g)为气体体积减小的反应,则缩小容器体积,压强增大平衡正向移动,与图一致,故D选;
故选D.
点评:本题考查化学平衡移动及图形分析,为高频考点,把握图中物质的量的变化判断平衡移动的方向为解答的关键,注意影响平衡移动的因素,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
用密度为1.32g/cm3的硫酸溶液逐滴滴入到氢氧化钡溶液中,直到沉淀恰好完全为止.已知生成沉淀的质量等于原硫酸溶液的质量,硫酸溶液中溶质的质量分数是( )
| A、42.1% |
| B、43.1% |
| C、44.1% |
| D、45.1% |
鉴别NO2气体和Br2蒸气,可用( )
| A、湿润的淀粉KI试纸 |
| B、AgNO3溶液 |
| C、水 |
| D、烧碱溶液 |
常温下,四种溶液的pH如下:
下列说法正确的是( )
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 硫酸 |
| pH | 11 | 11 | 3 | 3 |
| A、在①、②中分别加入适量的(NH4)2SO4晶体后,①的pH减小,②的pH不变 |
| B、将V1 mL④溶液与 V2 mL②溶液混合后,测得混合溶液pH=4,则V1:V2=9:11 |
| C、分别加水稀释10倍,四种溶液的pH大小顺序为:①>②>③>④ |
| D、将①、④两种溶液等体积混合,所得溶液中:c(NH4+)>c(SO42-)>c(OH-)>c(H+) |
盛装下列试剂的试剂瓶可用橡胶塞的是( )
| A、NaOH溶液 |
| B、氯仿 |
| C、酸性KMnO4溶液 |
| D、溴水 |
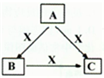 A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(其它产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(其它产物已略去),下列说法错误的是( )| A、若X为O2,则A可为硫化氢 |
| B、若X为KOH溶液,则A可能为AlCl3 |
| C、若X为Fe,则C可能为Fe(NO3)2 |
| D、若A、B、C均为焰色反应呈黄色的化合物,则X可能为Na |
下列叙述正确的是( )
| A、48g O3和O2的混合气体中含有6.02×1023个分子 |
| B、常温常压下,4.6g NO2气体含有1.806×1023个原子 |
| C、0.5mol?L-1 1L CuCl2溶液中含有3.01×1023个Cu2+ |
| D、标准状况下,3.36L H2O含有9.03×1023个分子H2O |
科学家在《Science》上发表论文,宣布发现了铝的超原子结构Al13和Al14,当这类超原子具有40个价电子(对于主族元素的原子,外围电子又称为价电子)时最稳定,在质谱仪上可检测到稳定到Al13-和Al142+.下列说法错误的是( )
| A、Al13和Al14互为同位素 |
| B、Al13超原子中Al原子间是通过共价键结合的 |
| C、Al13和Al的化学性质相似,都具有较强的还原性 |
| D、Al14和稀盐酸反应的化学方程式可表示为Al14+2HCl→Al14Cl2+H2↑ |